题目内容
莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法不正确的是( )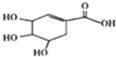

| A、分子式为C7H10O5 |
| B、1mol莽草酸与足量金属钠反应生成2molH2 |
| C、可发生加成反应、取代反应、氧化反应 |
| D、在水溶液中羧基和羟基均能电离出H+ |
考点:有机物的结构和性质
专题:
分析:该物质中含有羧基、醇羟基、碳碳双键,所以具有羧酸、烯烃、醇的性质,
A.分子中C原子形成四个共价键、O原子形成两个共价键、H原子形成一个共价键,据此判断分子式;
B.醇羟基、羧基能和Na反应生成氢气;
C.碳碳双键能发生加成反应、醇羟基和羧基能发生取代反应、有机物能发生氧化反应;
D.醇羟基不能发生电离.
A.分子中C原子形成四个共价键、O原子形成两个共价键、H原子形成一个共价键,据此判断分子式;
B.醇羟基、羧基能和Na反应生成氢气;
C.碳碳双键能发生加成反应、醇羟基和羧基能发生取代反应、有机物能发生氧化反应;
D.醇羟基不能发生电离.
解答:
解:该物质中含有羧基、醇羟基、碳碳双键,所以具有羧酸、烯烃、醇的性质,
A.分子中C原子形成四个共价键、O原子形成两个共价键、H原子形成一个共价键,该物质的分子式为C7H10O5,故A正确;
B.醇羟基、羧基能和Na反应生成氢气,反应中羧基或醇羟基与氢气的计量数之比为2:1,所以1mol莽草酸与足量金属钠反应生成2molH2,故B正确;
C.碳碳双键能发生加成反应、醇羟基和羧基能发生取代反应、有机物能发生氧化反应,醇羟基也能发生氧化反应,故C正确;
D.醇羟基不能发生电离,羧基能发生电离,故D错误;
故选D.
A.分子中C原子形成四个共价键、O原子形成两个共价键、H原子形成一个共价键,该物质的分子式为C7H10O5,故A正确;
B.醇羟基、羧基能和Na反应生成氢气,反应中羧基或醇羟基与氢气的计量数之比为2:1,所以1mol莽草酸与足量金属钠反应生成2molH2,故B正确;
C.碳碳双键能发生加成反应、醇羟基和羧基能发生取代反应、有机物能发生氧化反应,醇羟基也能发生氧化反应,故C正确;
D.醇羟基不能发生电离,羧基能发生电离,故D错误;
故选D.
点评:本题考查有机物结构和性质,为高考高频点,明确官能团及其性质的关系是解本题关键,注意并不是所有醇羟基都能发生氧化反应,熟练掌握常见有机物官能团及其性质.

练习册系列答案
相关题目
无色溶液中含有:①Na+、②Ba2+、③Cl-,④Br-、⑤SO32-、⑥SO42-、⑦Fe2+离子中的一种或几种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
根据上述实验现象,判断以下结论中正确的是( )
| 步骤 | 操作 | 现象 |
| ① | 用pH试纸检验 | 溶液的pH大于7 |
| ② | 向溶液中滴加氯水,再加入CCl4、振荡、静置 | CCl4层呈橙色 |
| ③ | 取②的上层溶液,加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
| ④ | 将③过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
| A、肯定含有的离子是①④⑤ |
| B、肯定没有的离子是②⑤⑦ |
| C、可能含有的离子是①②⑥ |
| D、不能确定的离子是①③⑥ |
一定质量的铁铝合金完全溶于过量的稀硝酸中,反应过程中共产生4.48LNO(标准状况下测定),若在反应后的溶液中加入足量的氢氧化物溶液,则生成沉淀的质量不可能是( )
| A、21.4g | B、18.7g |
| C、15.6g | D、7.8g |
下列说法正确的是( )
| A、常温下向饱和AgCl水溶液中加入盐酸,Ksp值变大 |
| B、用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| C、在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 |
| D、物质的溶解度随温度的升高而增加,物质的溶解都是吸热的 |
 25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示.下列说法正确的是( )
25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示.下列说法正确的是( )| A、稀释前,c(HX)=0.01 mol/L |
| B、稀释10倍,HX溶液的pH=3 |
| C、a、b两点:c(X-)>c(Cl-) |
| D、溶液的导电性:a>b |
下列叙述正确的是( )
| A、Na2SO3溶液中通入CO2溶液变浑浊,继续通入CO2至过量,浑浊消失 |
| B、均不能采取将溶液直接蒸干的方法制得AlCl3、Al2( SO4)3、Fe Cl3、Fe2( SO4)3 |
| C、Na、Mg、Cl是海水中的重要元素,从海水中制备这三种元素单质的反应都定存在氧化还原反应 |
D、元素X的单质及元素X与Y形成的化合物能按 关系发生转化,则X可为Fe或S 关系发生转化,则X可为Fe或S |
化学与生活密切相关,下列有关说法正确的是( )
| A、制作航天服的聚酯纤维属于新型无机非金属材料 |
| B、银器久置后表面变暗,是因为发生了电化学腐蚀 |
| C、Li是最轻的金属,也是活动性很强的金属,是制造电池的理想物质 |
| D、海水提取溴、煤的液化、焰色反应都发生了化学变化 |
 水系锂电池具有安全、环保和价格低廉等优点成为当前电池研究领域的热点.以钒酸钠(NaV3O8)为正极材料的电极反应式为:NaV3O8+xLi++xe-=NaLixV3O8,则下列说法不正确的是( )
水系锂电池具有安全、环保和价格低廉等优点成为当前电池研究领域的热点.以钒酸钠(NaV3O8)为正极材料的电极反应式为:NaV3O8+xLi++xe-=NaLixV3O8,则下列说法不正确的是( )| A、放电时,负极的电极反应式:Li-e-═Li+ |
| B、充电过程中Li+从阳极向阴极迁移 |
| C、充电过程中阳极的电极反应式为NaLixV3O8-xe-=NaV3O8+xLi+,NaLixV3O8中钒的化合价发生变化 |
| D、该电池可以用硫酸钠溶液作电解质 |