题目内容
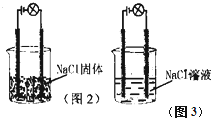 某化学兴趣小组进行化学实验,按照图2连接好线路发现灯泡不亮,按照图3连接好线路发现灯泡亮,由此得出的结论不正确的是( )
某化学兴趣小组进行化学实验,按照图2连接好线路发现灯泡不亮,按照图3连接好线路发现灯泡亮,由此得出的结论不正确的是( )| A、NaCl是电解质 |
| B、NaCl溶液是电解质 |
| C、NaCl在水溶液中电离出可以自由移动的离子 |
| D、NaCl溶液可以导电 |
考点:电解质在水溶液中的电离
专题:
分析:根据原电池的工作原理和构成条件:电解质溶液必须含有大量自由移动离子,电解质中阴阳离子的定向移动形成电流.
解答:
解:A、NaCl是强电解质,故A正确;
B、NaCl溶液属于混合物,不是电解质,故B错误;
C、NaCl在水溶液中电离出可以自由移动的钠离子和氯离子,故C正确;
D、NaCl溶液中含有大量的自由移动的氯离子和钠离子,所以可以导电,故D正确.
故选B.
B、NaCl溶液属于混合物,不是电解质,故B错误;
C、NaCl在水溶液中电离出可以自由移动的钠离子和氯离子,故C正确;
D、NaCl溶液中含有大量的自由移动的氯离子和钠离子,所以可以导电,故D正确.
故选B.
点评:本题考查学生电解池的构成条件中的:含有电解质溶液或是熔融的电解质这一条知识,注意知识的迁移应用能力的培养是关键,难度中等.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
列有关物质用途的说法中,正确的是( )
| A、硅可用作绝缘材料 |
| B、液氨可用作制冷剂 |
| C、氯化钠常用于中和胃酸 |
| D、铝制容器常用于盛装稀硫酸 |
12 6 |
12 6 |
| A、12 | B、6 | C、18 | D、4 |
 迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如下图.下列叙述正确的是( )
迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如下图.下列叙述正确的是( )| A、迷迭香酸属于芳香烃 |
| B、1mol迷迭香酸最多能和1mol氢气发生加成反应 |
| C、迷迭香酸可以发生水解反应但不能发生酯化反应 |
| D、迷迭香酸中只有一个手性碳原子 |
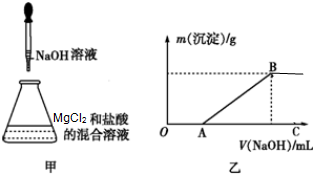 某同学称取一定量的MgCl2固体配成溶液,在该溶液中先加入一定量的稀盐酸,然后逐滴加入NaOH溶液(如图甲所示)
某同学称取一定量的MgCl2固体配成溶液,在该溶液中先加入一定量的稀盐酸,然后逐滴加入NaOH溶液(如图甲所示)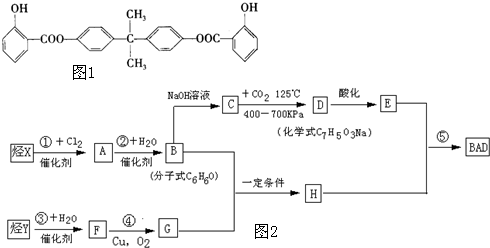

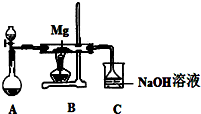 SiO2、SO2和CO2都是酸性氧化物,它们的化学性质有一定的相似性;Mg和Na的化学性质也有一定相似性.某兴趣小组用如图所示装置进行Mg与
SiO2、SO2和CO2都是酸性氧化物,它们的化学性质有一定的相似性;Mg和Na的化学性质也有一定相似性.某兴趣小组用如图所示装置进行Mg与