题目内容
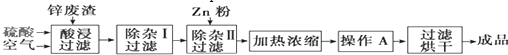
工业上常回收冶炼锌废渣中的锌(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质),并用来生产ZnSO4?6H2O晶体,其工艺流程如下,有关氢氧化物沉淀时的pH如下表.
(1)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有 .
(2)在“除杂Ⅰ”步骤中,需再加入适量H2O2溶液的目的是 .为使Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为 .为控制上述PH范围可选择加入的试剂或药品是 .
A.ZnO B.氨水 C.固体NaOH D.ZnCO3
(3)在“除杂Ⅱ”步骤中,加入Zn粉的作用是 .“操作A”的名称是 .
(4)常温下,已知Ksp〔Cu(OH)2〕=2×10-20,某CuSO4溶液里c(Cu2+)=0.02mol?L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于 .

| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 5.4 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 8.0 |
(2)在“除杂Ⅰ”步骤中,需再加入适量H2O2溶液的目的是
A.ZnO B.氨水 C.固体NaOH D.ZnCO3
(3)在“除杂Ⅱ”步骤中,加入Zn粉的作用是
(4)常温下,已知Ksp〔Cu(OH)2〕=2×10-20,某CuSO4溶液里c(Cu2+)=0.02mol?L-1,如果要生成Cu(OH)2沉淀,则应调整溶液pH大于
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:冶炼锌废渣中的锌(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质),加入硫酸通入空气酸浸过滤后得到滤液含有Zn2+、Fe3+、Fe2+、Cu2+、Al3+,加入过氧化氢氧化亚铁离子为铁离子,调节溶液PH使铁离子、铝离子全部沉淀,过滤后滤液中加入锌除去铜离子,过滤得到硫酸锌溶液,加热蒸发,浓缩结晶,过滤洗涤得到ZnSO4?6H2O晶体;
(1)依据过滤操操作需要的玻璃仪器;
(2)过氧化氢是绿色氧化剂氧化亚铁离子为铁离子,通过调节溶液PH除去铁离子、铝离子而氢氧化锌不沉淀,结合图表数据判断需要的PH和试剂,注意加入物质能调节溶液PH,不能引入新的杂质;
(3)分析可知加入锌还原铜离子除去,硫酸锌溶液得到晶体的方法是利用加热蒸发浓缩,冷却结晶得到;
(4)依据沉淀的溶度积计算;
(1)依据过滤操操作需要的玻璃仪器;
(2)过氧化氢是绿色氧化剂氧化亚铁离子为铁离子,通过调节溶液PH除去铁离子、铝离子而氢氧化锌不沉淀,结合图表数据判断需要的PH和试剂,注意加入物质能调节溶液PH,不能引入新的杂质;
(3)分析可知加入锌还原铜离子除去,硫酸锌溶液得到晶体的方法是利用加热蒸发浓缩,冷却结晶得到;
(4)依据沉淀的溶度积计算;
解答:
解:冶炼锌废渣中的锌(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质),加入硫酸通入空气酸浸过滤后得到滤液含有Zn2+、Fe3+、Fe2+、Cu2+、Al3+,加入过氧化氢氧化亚铁离子为铁离子,调节溶液PH使铁离子、铝离子全部沉淀,过滤后滤液中加入锌除去铜离子,过滤得到硫酸锌溶液,加热蒸发,浓缩结晶,过滤洗涤得到ZnSO4?6H2O晶体;
(1)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有烧杯、玻璃棒、漏斗;
故答案为:烧杯、玻璃棒、漏斗;
(2)在“除杂Ⅰ”步骤中,需再加入适量H2O2溶液的目的是将Fe2+完全氧化为Fe3+,便于完全沉淀;依据图表数据分析,为使Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为5.2~5.4;为控制上述PH范围可选择加入的试剂或药品不能引入新的杂质,氨水会引入铵根离子,固体氢氧化钠会引入钠离子,ZnO、ZnCO3,会降低溶液PH且不引入新的杂质;
故答案为:将Fe2+完全氧化为Fe3+,5.2~5.4;AD;
(3)在“除杂Ⅱ”步骤中,加入Zn粉的作用是除去溶液中的Cu2+.“操作A”的名称是硫酸锌溶液得到晶体的方法是利用加热蒸发浓缩,冷却结晶得到;
故答案为:除去溶液中的Cu2+;冷却结晶;
(4)常温下,已知Ksp〔Cu(OH)2〕=2×10-20,某CuSO4溶液里c(Cu2+)=0.02mol?L-1,如果要生成Cu(OH)2沉淀,Q≥Ksp,Ksp〔Cu(OH)2〕=c(Cu2+)×c2(OH-)=2×10-20,c(OH-)=
=
=10-9mol/L,c(H+)=10-5mol/L,PH=5,则应调整溶液pH大,5;
故答案为:5;
(1)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有烧杯、玻璃棒、漏斗;
故答案为:烧杯、玻璃棒、漏斗;
(2)在“除杂Ⅰ”步骤中,需再加入适量H2O2溶液的目的是将Fe2+完全氧化为Fe3+,便于完全沉淀;依据图表数据分析,为使Fe(OH)3、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为5.2~5.4;为控制上述PH范围可选择加入的试剂或药品不能引入新的杂质,氨水会引入铵根离子,固体氢氧化钠会引入钠离子,ZnO、ZnCO3,会降低溶液PH且不引入新的杂质;
故答案为:将Fe2+完全氧化为Fe3+,5.2~5.4;AD;
(3)在“除杂Ⅱ”步骤中,加入Zn粉的作用是除去溶液中的Cu2+.“操作A”的名称是硫酸锌溶液得到晶体的方法是利用加热蒸发浓缩,冷却结晶得到;
故答案为:除去溶液中的Cu2+;冷却结晶;
(4)常温下,已知Ksp〔Cu(OH)2〕=2×10-20,某CuSO4溶液里c(Cu2+)=0.02mol?L-1,如果要生成Cu(OH)2沉淀,Q≥Ksp,Ksp〔Cu(OH)2〕=c(Cu2+)×c2(OH-)=2×10-20,c(OH-)=
|
|
故答案为:5;
点评:本题考查了物质分离实验过程和分离原理的理解应用,除杂试剂选择和提纯物质方法,沉淀溶解平衡的计算应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
常温下,能用铁制容器盛放的液体是( )
| A、稀盐酸 |
| B、稀硝酸 |
| C、FeCl3溶液 |
| D、浓H2SO4 |
下列有关氧化还原反应的叙述中,正确的是( )
| A、一定有氧元素参加 |
| B、一定有电子转移(得失或偏移) |
| C、氧化反应一定先于还原反应发生 |
| D、氧化剂本身发生氧化反应 |
25℃,弱酸的电离平衡常数Ka如表所示,下列说法正确的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10-5 | 4.9×10-10 | K1:4.3×10-7 K2:5.6×10-11 |
| A、pH相同的三种溶液物质的量浓度关系:c(Na2CO3)>c(NaCN)>c(CH3COONa) |
| B、a L 0.1mol?L-1CH3COOH与b L 0.1mol?L-1NaOH溶液混合后所得溶液中pH>7,则a一定小于或等于b |
| C、物质的量浓度和体积均相同的CH3COONa和NaOH两种溶液,已知前者溶液中离子数目为n1,后者溶液中离子数目为n2,则n1>n2 |
| D、物质的量浓度相同NaHCO3和Na2CO3的混合溶液中:2c(H+)-2c(OH-)=c(CO32-)-c(HCO3-)-c(H2CO3) |
将CO2气体通入下列溶液中,无沉淀生成的是( )
| A、Na2SiO3溶液 |
| B、BaCl2溶液 |
| C、NaAlO2溶液 |
| D、硬脂酸钠溶液 |
只由两种元素组成的化合物,其中一种元素是氢元素,这类化合物称氢化物.下列物质属于氢化物的是( )
| A、H2CO3 |
| B、H2SO4 |
| C、NaH |
| D、HClO |
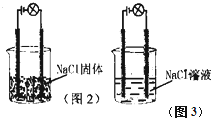 某化学兴趣小组进行化学实验,按照图2连接好线路发现灯泡不亮,按照图3连接好线路发现灯泡亮,由此得出的结论不正确的是( )
某化学兴趣小组进行化学实验,按照图2连接好线路发现灯泡不亮,按照图3连接好线路发现灯泡亮,由此得出的结论不正确的是( )| A、NaCl是电解质 |
| B、NaCl溶液是电解质 |
| C、NaCl在水溶液中电离出可以自由移动的离子 |
| D、NaCl溶液可以导电 |