题目内容
12.某烃的蒸气密度是氢气的28倍.此烃完全燃烧后的产物经过浓硫酸后,浓硫酸增重3.6克,余下气体经过氢氧化钠溶液后,氢氧化钠溶液增重8.8克.计算:(1)此烃的分子式?
(2)此烃可使高锰酸钾褪色,写出该烃的可能的同分异构体,并命名.
分析 某烃的蒸气密度是氢气的28倍,则相对分子质量为56,此烃完全燃烧后的产物经过浓硫酸后,浓硫酸增重3.6克,为水的质量,可知n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,余下气体经过氢氧化钠溶液后,氢氧化钠溶液增重8.8克,为二氧化碳的质量,n(CO2)=$\frac{8.8g}{44g/mol}$=0.2mol,计算C、H原子个数比值结合相对分子质量可确定分子式,此烃可使高锰酸钾褪色,说明含有碳碳不饱和键,以此解答该题.
解答 解:(1)某烃的蒸气密度是氢气的28倍,则相对分子质量为56,此烃完全燃烧后的产物经过浓硫酸后,浓硫酸增重3.6克,为水的质量,可知n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,余下气体经过氢氧化钠溶液后,氢氧化钠溶液增重8.8克,为二氧化碳的质量,n(CO2)=$\frac{8.8g}{44g/mol}$=0.2mol,
则n(C):n(H)=0.2mol:0.2mol×2=1:2,
最简式为CH2,
则分子式为C4H8,
答:此烃的分子式为C4H8;
(2)此烃可使高锰酸钾褪色,说明含有碳碳不饱和键,应为丁烯,可能的同分异构体有CH2=CHCH2CH3,名称为1-丁烯;CH3CH=CHCH3,名称为2-丁烯;CH2=C(CH3)2,名称为2-甲基-1-丙烯,
答:CH2=CHCH2CH3,名称为1-丁烯;CH3CH=CHCH3,名称为2-丁烯;CH2=C(CH3)2,名称为2-甲基-1-丙烯.
点评 本题考查有机物的推断,为高频考点,侧重于学生的分析、计算能力的考查,注意把握有机物分子式确定,比较基础,可以根据原子守恒计算C、H原子数目确定A的分子式,有利于基础知识的巩固.

练习册系列答案
相关题目
2.根据如图所示情况,判断下列说法中正确的是( )
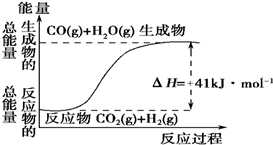

| A. | 其热化学方程式为:CO(g)+H2O(g)═CO2(g)+H2(g)△H=41kJ•mol-1 | |
| B. | 该反应为吸热反应 | |
| C. | 该反应为放热反应 | |
| D. | 若当H2O为液态时反应热为△H2,则△H2>△H |
3.固体粉末X中可能含有FeO、Fe2O3、MnO2、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3、NaNO2中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如图.根据实验,以下说法正确的是( )
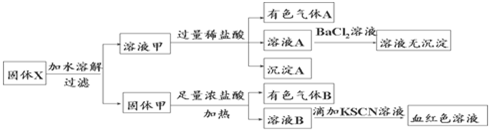

| A. | 溶液甲中一定含有K2SiO3、NaNO2、可能含有KAlO2、K2CO3 一定不含有K2SO3 | |
| B. | 沉淀A为H2SiO3 | |
| C. | 气体A和气体B一定均为纯净物 | |
| D. | 原混合物中一定含有Fe2O3 |
4.下列叙述正确的是( )
| A. | 丙烷分子中3个碳原子一定在同一条直线上 | |
| B. | 丙烯分子中3个碳原子都在同一平面 | |
| C. | 乙烷分子中碳原子和全部氢原子可能在同一平面上 | |
| D. | 2-丁烯分子中4个碳原子在同一平面上 |
1.将SO2通入BaCl2溶液至饱和,未见白色沉淀出现,继续通入另一种气体,观察到有白色沉淀出现,则通入的气体不可能是( )
| A. | NH3 | B. | HCl | C. | Cl2 | D. | NO2 |
2.自来水常用氯气消毒,某实验室用自来水配制下列物质的溶液,不会产生明显药品变质问题的是( )
| A. | FeCl2 | B. | Na2SO4 | C. | NaOH | D. | AlCl3 |
 实验室配制250mL 0.100mol/L氯化钠溶液:
实验室配制250mL 0.100mol/L氯化钠溶液: .
.