题目内容
20.原子种类由质子数和中子数决定;元素种类由质子数决定;元素的化学性质主要由该元素原子的最外层电子数决定.分析 核素是具有一定数目质子和一定数目中子的一种原子;
质子数相同的同一类原子统称为元素;
化学性质主要由该元素原子的最外层电子数决定.
解答 解:核素是具有一定数目质子和一定数目中子的一种原子,则原子种类由质子数和中子数共同决定;
元素是具有相同核内质子数(或核电荷数)的一类原子的总称,则元素种类由质子数决定;
化学性质主要由价电子决定,而主族元素价电子一般就是最外层电子,而副族元素大多还包括次外层的一些电子,
故答案为:质子数和中子数;质子数;最外层电子数.
点评 本题考查了原子的构成,题目难度不大,侧重考查学生对原子结构的掌握程度.

练习册系列答案
相关题目
11.常温下将盛有10mL NO2和10mL NO的混合气体的试管倒立于水槽中,并向其中通入O2一段时间后,试管内还剩余2mL气体,则通入O2的体积为( )
| A. | 8mL | B. | 8.5mL | C. | l0mL | D. | 13mL |
8.分子里所有原子都在同一平面上的是( )
| A. | 甲烷、乙烯、乙炔 | B. | 乙烯、苯、乙炔 | C. | 乙醇、乙醛、乙酸 | D. | 乙烯、苯、甲苯 |
15.下列物质中,制取时不需用石灰石作原料的是( )
| A. | 硅酸 | B. | 水泥 | C. | 玻璃 | D. | 生石灰 |
9.某元素的一种同位素X的原子质量数为A,含N个中子,X的最高价氧化物为XO3,则在a g X的气态氢化物中所含质子的物质的量是( )
| A. | $\frac{a}{A+3}$(A-N+3)mol | B. | $\frac{a}{A}$(A-N)mol | C. | $\frac{a}{A+2}$(A-N+2)mol | D. | $\frac{a}{A+3}$(A-N)mol |
10.常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:
请回答:
(1)从①组情况分析,HA是强酸还是弱酸弱酸(填“强酸”或“弱酸”);
(2)①组实验所得混合溶液中由水电离出的c(OH-)=10-5mol•L-1.
(3)②组情况表明,c大于0.2mol/L(选填“大于”、“小于”或“等于”).混合液中离子浓度c(A-)与c(Na+)的大小关系是等于.
(4)从③组实验结果分析,说明HA的电离程度大于NaA的水解程度(选填“大于”、“小于”或“等于”),该混合溶液中离子浓度由大到小的顺序是c(A-)>c(Na+)>c(H+)>c(OH-).
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
(1)从①组情况分析,HA是强酸还是弱酸弱酸(填“强酸”或“弱酸”);
(2)①组实验所得混合溶液中由水电离出的c(OH-)=10-5mol•L-1.
(3)②组情况表明,c大于0.2mol/L(选填“大于”、“小于”或“等于”).混合液中离子浓度c(A-)与c(Na+)的大小关系是等于.
(4)从③组实验结果分析,说明HA的电离程度大于NaA的水解程度(选填“大于”、“小于”或“等于”),该混合溶液中离子浓度由大到小的顺序是c(A-)>c(Na+)>c(H+)>c(OH-).
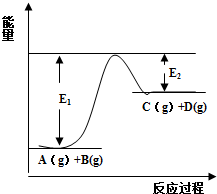 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题.