题目内容
13.对0.5mol•L-1的氨水,分别加入下列各物质或进行某项操作:A、4mol•L-1氨水、B、纯水、C、少量NH4Cl晶体、D、少量浓醋酸、E、少量NaOH粉末、F、少量FeCl3晶体、G、加热,
用序号填写下列空白:
(1)能使pH减小,c(NH4+)增大的是CDF,
(2)能使pH增大,c(NH4+)减少的是E,
(3)能使pH增大,c(NH4+)也增大的是AG,
(4)能使pH减小,c(NH4+)也减小的是B.
分析 (1)加入含有铵根离子的物质能抑制一水合氨电离且溶液中c(NH4+)增大,加入和OH-反应的物质能促进一水合氨电离,且溶液中c(NH4+)增大,但溶液的pH减小;
(2)加入含有OH-的物质能抑制一水合氨电离,且溶液中c(OH-)增大;
(3)加入浓氨水或升高温度,溶液中c(NH4+)及溶液的pH都增大;
(4)加水稀释能促进一水合氨电离,但溶液中c(NH4+)、c(OH-)都减小.
解答 解:(1)加入含有铵根离子的物质能抑制一水合氨电离且溶液中c(NH4+)增大,加入和OH-反应的物质能促进一水合氨电离,且溶液中c(NH4+)增大,但溶液的pH减小,符合条件的有氯化铵晶体、浓醋酸、少量FeCl3晶体,故答案为:CDF;
(2)加入含有OH-的物质能抑制一水合氨电离,且溶液中c(OH-)增大,溶液的pH增大,符合条件的为NaOH,故答案为:E;
(3)加入浓氨水或升高温度,溶液中c(NH4+)及溶液的pH都增大,则符合条件的有AG,故答案为:AG;
(4)加水稀释能促进一水合氨电离,但溶液中c(NH4+)、c(OH-)都减小,所以溶液的pH减小,则符合条件的为B,故答案为:B.
点评 本题考查弱电解质的电离,为高频考点,侧重考查学生分析判断能力,明确弱电解质电离影响因素是解本题关键,注意:加水稀释促进一水合氨电离但一水合氨电离增大程度小于溶液体积增大程度导致溶液中除了c(H+)外所有离子浓度都减小,为易错点.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
4.2008年北京奥运会的“祥云”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述中不正确的是( )
| A. | 分子中碳原子不在一条直线上 | B. | 比丁烷更易液化 | ||
| C. | 1mol丙烷完全燃烧需消耗氧气5mol | D. | 光照下能够发生取代反应 |
1.甲烷分子中的四个氢原子都可以被取代.若甲烷分子中的四个氢原子都被苯基取代,则可得到分子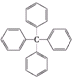 .对该分子的描述正确的是( )
.对该分子的描述正确的是( )
 .对该分子的描述正确的是( )
.对该分子的描述正确的是( )| A. | 分子式为C25H20 | B. | 其不是芳香烃 | ||
| C. | 所有碳原子都在同一平面上 | D. | 该物质为脂环烃 |
18.下列说法不正确的是( )
| A. | 纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应 | |
| B. | 分子式是C3H8O的所有同分异构体共3种 | |
| C. | 用乙醇和浓H2SO4制备乙烯时,不可用水浴加热控制反应的温度 | |
| D. | 迷迭香酸结构如图: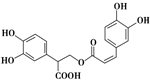 1 mol 迷迭香酸最多能和含6 mol NaOH的水溶液完全反应 1 mol 迷迭香酸最多能和含6 mol NaOH的水溶液完全反应 |
5.有a mol C2H4跟b mol H2在密闭容器中,催化剂存在下反应若干时间后生成了c mol C2H6,除去催化剂后,将此混合气体完全燃烧生成CO2 和H2O,所需氧气的物质的量应是( )
| A. | (3a+b) mol | B. | (3a+0.5b-3.5c) mol | ||
| C. | ( 3a+b+3.5c) mol | D. | (3a+0.5b) mol |
2.取等质量两种烃A、B完全燃烧,生成的CO2与消的O2的量相同,这两种烃之间的关系正确的是( )
| A. | 一定互为同分异构体 | B. | 一定互为同系物 | ||
| C. | 实验式一定相同 | D. | 只能是同种物质 |
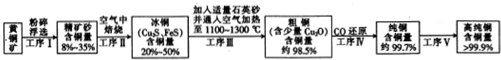
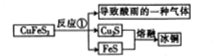
 氯元素的单质及其化合物在生产生活中都很重要.回答下列问题:
氯元素的单质及其化合物在生产生活中都很重要.回答下列问题: .
.