题目内容
表面被部分氧化成过氧化钠的一小块钠,质量为2.48g,放入足量水中,收集所产生的气体,点燃该气体,气体恰好完全反应,求原钠块中过氧化钠 g.
考点:化学方程式的有关计算
专题:计算题
分析:反应的有关方程式为:2Na+2H2O=2NaOH+H2↑,2Na2O2+2H2O=4NaOH+O2↑,2H2+O2
2H2O,根据总质量及气体恰好反应,列式计算.
| ||
解答:
解:设混合物中含有xmolNa,ymolNa2O2,
反应的有关方程式为:2Na+2H2O=2NaOH+H2↑,
2Na2O2+2H2O=4NaOH+O2↑,
2H2+O2
2H2O,
充分反应后产生的两种气体可恰好完全反应,即n(H2):n(O2)=2:1,
则有:
解之得:
原固体混合物中过氧化钠的质量为:0.02mol×78g/mol=1.56g,
故答案为:1.56g.
反应的有关方程式为:2Na+2H2O=2NaOH+H2↑,
2Na2O2+2H2O=4NaOH+O2↑,
2H2+O2
| ||
充分反应后产生的两种气体可恰好完全反应,即n(H2):n(O2)=2:1,
则有:
|
解之得:
|
原固体混合物中过氧化钠的质量为:0.02mol×78g/mol=1.56g,
故答案为:1.56g.
点评:本题考查混合物的计算,题目难度不大,注意金属钠与过氧化钠与水反应的性质,抓住题中充分反应后产生的两种气体可恰好完全反应的特点.

练习册系列答案
相关题目
向含有7.4g Ca(OH)2的澄清石灰水中通入CO2气体后,得到8g白色沉淀,则通入的CO2气体的物质的量为( )
| A、0.08mol |
| B、0.10mol |
| C、0.12mol |
| D、0.18mol |
将一定质量的Mg、Zn、Al混合物与足量稀H2SO4反应,生成H2 2.8L(标准状况),原混合物的质量一定不可能是( )
| A、5g | B、4g | C、8g | D、10g |
某温度下,反应H2(g)+I2(g)?2HI(g);△H>0.在一带有活塞的密闭容器中达到平衡,下列说法中不正确的是( )
| A、恒温,压缩体积,平衡不移动,混合气体颜色加深 |
| B、恒压,充入HI(g),开始时正反应速率减小 |
| C、恒容,升高温度,正反应速率减小 |
| D、恒容,充入H2,I2(g)的体积分数降低 |
下列物质的用途与其化学性质相关的是( )
| A、用氮气作食品包装袋的填充气 |
| B、用金刚石切割玻璃 |
| C、用活性炭作净水剂 |
| D、用金属铝作导线 |
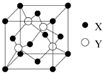 元素X位于第四周期,其基态原子的内层轨道全部排满电子,最外层电子数为2.元素Y基态原子的3p轨道有4个电子.元素Z的原子最外层电子数是内层的3倍.
元素X位于第四周期,其基态原子的内层轨道全部排满电子,最外层电子数为2.元素Y基态原子的3p轨道有4个电子.元素Z的原子最外层电子数是内层的3倍. (1)将4molSO2和2molO2充入2L的密闭容器中,在一定条件下发生反应,经10s后达到平衡,测得SO3的浓度为0.6mol?L-1,请回答下列问题:
(1)将4molSO2和2molO2充入2L的密闭容器中,在一定条件下发生反应,经10s后达到平衡,测得SO3的浓度为0.6mol?L-1,请回答下列问题: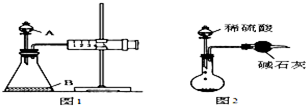 学校实验室现有含少量NaCl杂质的Na2CO3固体样品,某化学兴趣小组的同学决定测定样品Na2CO3的质量分数,甲、乙两位同学分别设计出下列两种实验方案:
学校实验室现有含少量NaCl杂质的Na2CO3固体样品,某化学兴趣小组的同学决定测定样品Na2CO3的质量分数,甲、乙两位同学分别设计出下列两种实验方案: