题目内容
下列说法正确的是( )
| A、Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换 |
| B、Na2O2中阴阳离子数数目之比为1:1 |
| C、Cl2与SO2均能使品红褪色,说明二者均有氧化性 |
| D、NO能够与人体里的血红蛋白结合,造成人体缺氧中毒 |
考点:铁的化学性质,氯气的化学性质,氮的氧化物的性质及其对环境的影响
专题:
分析:A.铁与稀硝酸反应生成二氧化氮、硝酸铁和水;
B.依据过氧化钠中含有钠离子和过氧根离子解答;
C.二氧化硫能与品红结合成无色物质,使品红溶液褪色;
D.NO是有毒的气体,呼入人体内会和人体血红蛋白结合,造成人体缺氧中毒.
B.依据过氧化钠中含有钠离子和过氧根离子解答;
C.二氧化硫能与品红结合成无色物质,使品红溶液褪色;
D.NO是有毒的气体,呼入人体内会和人体血红蛋白结合,造成人体缺氧中毒.
解答:
解:A.铁与稀硝酸反应生成二氧化氮、硝酸铁和水,不属于置换反应,故A错误;
B.Na2O2中含有2个钠离子和1个过氧根离子,故B错误;
C.SO2能使品红溶液褪色,原因是二氧化硫能与有色物质结合成无色物质,不是因为氧化性,故C错误;
D.NO是有毒的气体,呼入人体内会和人体血红蛋白结合,造成人体缺氧中毒,故D正确;
故选:D.
B.Na2O2中含有2个钠离子和1个过氧根离子,故B错误;
C.SO2能使品红溶液褪色,原因是二氧化硫能与有色物质结合成无色物质,不是因为氧化性,故C错误;
D.NO是有毒的气体,呼入人体内会和人体血红蛋白结合,造成人体缺氧中毒,故D正确;
故选:D.
点评:本题考查了元素和化合物的性质,明确硝酸、二氧化硫、一氧化氮的性质,明确过氧化钠的结构是解题关键,题目难度不大.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
容积可变的密闭容器中盛有适量的N2和H2的混合气体,在一定条件下反应N2+3H2?2NH3,达平衡时容积为V L,混合气体中氨气占总体积的20%,若压强温度不变,下列推论不正确的是( )
| A、原N2、H2混合气体为1.0V L |
| B、原N2、H2混合气体为1.2V L |
| C、参加反应的N2为0.1V L |
| D、原混合气体中N2、H2体积比为1:3 |
下列实验操作中错误的是( )
| A、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、蒸发结晶时应将溶液蒸干 |
| D、称量NaOH,称量物放在小烧杯中置于托盘天平的左盘,砝码放在托盘天平的右盘中 |
下列实验操作中不会使用到玻璃棒的是( )
| A、分离食盐水中的泥沙 |
| B、浓硫酸的稀释 |
| C、测定某溶液的pH值 |
| D、蒸馏法分离酒精和水 |
室温时,盐酸和硫酸的混合溶液20ml,向混合溶液中逐滴加入0.05mol?L-1Ba(OH)2溶液时,生成的BaSO4和pH的变化如图所示(不考虑溶液混合时体积的变化).下列说法正确的是( )
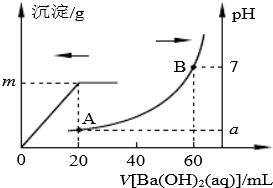

| A、图中A点对应溶液的pH=l |
| B、生成沉淀的最大质量m=2.33 g |
| C、原混合溶液中盐酸物质的量浓度为0.1 mol?L-1 |
| D、当V[Ba(OH)2(aq)]=10 mL时,发生反应的离子方程式为:Ba2++SO42-═BaSO4↓ |
 某有机物与H2按1:1的物质的量之比加成后生成的产物结构为:则该有机物可能的结构有(羟基与碳碳双键相连的结构不稳定,不考虑其存在)( )
某有机物与H2按1:1的物质的量之比加成后生成的产物结构为:则该有机物可能的结构有(羟基与碳碳双键相连的结构不稳定,不考虑其存在)( )| A、3种 | B、4种 | C、5种 | D、6种 |
 某兴趣小组设计如图微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表A指针偏转.下列说法正确的是( )
某兴趣小组设计如图微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表A指针偏转.下列说法正确的是( )A、断开K2,闭合K1时,总反应的离子方程式为2H++2Cl-
| ||||
| B、断开K2、闭合K1时,石墨电极附近溶液变红 | ||||
| C、断开K1、闭合K2时,铜电极上的电极反应为Cl2+2e-═2Cl- | ||||
| D、断开K1、闭合K2时,石墨电极作正极 |
 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此回答下列问题:
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此回答下列问题:

 ,参照上述合成路线中的有关信息,写出由对甲苯酚为原料合成
,参照上述合成路线中的有关信息,写出由对甲苯酚为原料合成 的合成流程图(其它试剂自选)
的合成流程图(其它试剂自选)