题目内容
 某兴趣小组设计如图微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表A指针偏转.下列说法正确的是( )
某兴趣小组设计如图微型实验装置.实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表A指针偏转.下列说法正确的是( )A、断开K2,闭合K1时,总反应的离子方程式为2H++2Cl-
| ||||
| B、断开K2、闭合K1时,石墨电极附近溶液变红 | ||||
| C、断开K1、闭合K2时,铜电极上的电极反应为Cl2+2e-═2Cl- | ||||
| D、断开K1、闭合K2时,石墨电极作正极 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.断开K2,闭合K1时,是电解池装置,两极均有气泡产生,说明两极产生的气体分别是氢气和氯气;
B.断开K2,闭合K1时,是电解池装置,两极均有气泡产生,石墨做阳极,溶液中氯离子离子失电子发生氧化反应,铜做阴极,氢离子得到电子发生还原反应;
C.断开K1,闭合K2时,发现电流表指针偏转,证明是原电池反应,形成氢氯燃料电池,铜做负极氢气失电子发生氧化反应;
D.断开K1,闭合K2时,形成原电池,原电池中阳离子向正极移动.
B.断开K2,闭合K1时,是电解池装置,两极均有气泡产生,石墨做阳极,溶液中氯离子离子失电子发生氧化反应,铜做阴极,氢离子得到电子发生还原反应;
C.断开K1,闭合K2时,发现电流表指针偏转,证明是原电池反应,形成氢氯燃料电池,铜做负极氢气失电子发生氧化反应;
D.断开K1,闭合K2时,形成原电池,原电池中阳离子向正极移动.
解答:
解:断开K2、闭合K1时,装置为电解池,两极均有气泡产生,则总反应为2Cl-+2H2O
H2↑+2OH-+Cl2↑,石墨为阳极,铜为阴极,因此石墨电极处产生Cl2,在铜电极处产生H2,铜电极附近产生OH-,溶液变红,故A、B两项均错误;
断开K1、闭合K2时,装置为原电池,铜电极上的电极反应为H2-2e-+2OH-=2H2O,其为负极,而石墨上的电极反应为Cl2+2e-=2Cl-,其为正极,故C项错误,D项正确.
故选D.
| ||
断开K1、闭合K2时,装置为原电池,铜电极上的电极反应为H2-2e-+2OH-=2H2O,其为负极,而石墨上的电极反应为Cl2+2e-=2Cl-,其为正极,故C项错误,D项正确.
故选D.
点评:本题综合考查电解池和原电池知识,注意把握电化学工作原理,为高考常见题型,侧重于学生的分析能力的考查,有利于培养学生的良好的科学素养,难度中等.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
下列说法正确的是( )
| A、Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换 |
| B、Na2O2中阴阳离子数数目之比为1:1 |
| C、Cl2与SO2均能使品红褪色,说明二者均有氧化性 |
| D、NO能够与人体里的血红蛋白结合,造成人体缺氧中毒 |
在一定条件下,分别以高锰酸钾、氯酸钾、过氧化氢为原料制取氧气,当制得同温同压下相同体积的氧气时,三个反应中转移的电子数之比为( )
| A、1:1:2 |
| B、2:2:1 |
| C、2:3:1 |
| D、4:3:2 |
下列事实不能用勒夏特列原理解释的是( )
| A、黄绿色的氯水光照后颜色变浅 |
| B、NO2(g)+SO2(g)?SO3(g)+NO(g),对该平衡体系加压后颜色加深 |
| C、由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅 |
| D、在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去 |
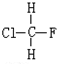 与
与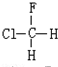
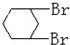 与
与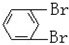
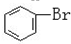 与
与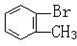
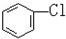 与
与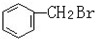
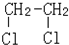 与CH3-CH2Cl.
与CH3-CH2Cl. (1)可用如图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为如图.请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系.
(1)可用如图示的方法表示不同反应类型之间的关系.如分解反应和氧化还原反应可表示为如图.请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系.