题目内容
19.金属钠分别与下列物质的溶液反应时,既有气体放出又有白色沉淀生成的是( )| A. | 盐酸 | B. | 氯化钠 | C. | 氯化铜 | D. | 氯化镁 |
分析 将钠投入溶液中,钠和水反应生成氢氧化钠和氢气,氢氧化钠和部分盐能发生复分解反应,根据产物的可溶性以及沉淀的颜色判断.
解答 解:A.钠和HCl反应生成氯化钠和氢气,所以只能生成气体,不会产生沉淀,故A错误;
B.钠和水反应生成可溶性的氢氧化钠和氢气,氢氧化钠与NaCl不反应,所以只能生成气体,不会产生沉淀,故B错误;
C.钠和水反应生成可溶性的氢氧化钠和氢气,氢氧化钠与氯化铜反应生成氢氧化铜沉淀,不是白色,故C错误;
D.钠和水反应生成可溶性的氢氧化钠和氢气,氢氧化钠与氯化镁反应生成氢氧化镁白色沉淀,故D正确.
故选D.
点评 本题考查元素化合物的性质,比较简单,钠与碱、盐的反应中首先考虑与溶液中的水反应,然后再看生成的氢氧化钠能否与碱、盐本身反应.

练习册系列答案
相关题目
12.日常生活中的下列物质,属于人工合成材料的是( )
| A. | 羊毛 | B. | 棉线 | C. | 涤纶 | D. | 真丝巾 |
10.下列关于化学用语的表示正确的是( )
| A. | 质子数为17、中子数为20的氯(Cl)原子:${\;}_{17}^{20}$Cl | |
| B. | CO2电子式: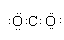 | |
| C. | 镁离子的结构示意图: | |
| D. | CCl4分子的比例模型: |
14.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,8 g O2含有5NA个电子 | |
| B. | 1 L 1.0 mol•L-1NaAlO2溶液中含有氧原子数为2NA | |
| C. | 标准状况下,2.24 L CCl4中含有的分子数为0.1NA | |
| D. | 精炼铜的过程中,当阴极析出32 g铜时转移的电子数为NA |
4.同温同压下,等质量的CO和CO2气体相比较,下列叙述中正确的是( )
| A. | 所含碳原子数比为1:1 | B. | 体积比为1:1 | ||
| C. | 密度比为7:11 | D. | 分子数比为7:11 |
11.下列物质按电解质、非电解质、混合物排序正确的是( )
| A. | 五水硫酸铜、SO2、空气 | B. | NH3、Cu、空气 | ||
| C. | 盐酸、硫酸、胶体 | D. | 氨水、食盐、酒精 |
9.汽车排放的尾气中含有NO2,NO2是城市大气污染的主要污染物之一.在日光照射下,NO2发生一系列光化学烟雾的循环反应,从而不断产生O3,加重空气污染.反应过程为①2NO2-→2NO+2O;②2NO+O2- →2NO2;③O+O2- →O3.下列对该反应过程及产物叙述正确的是( )
| A. | NO2只起还原剂作用 | B. | NO2起催化剂作用 | ||
| C. | NO2只起氧化剂作用 | D. | O3与O2互为同分异构体 |