题目内容
9.只用一种试剂就能区别NaCl溶液、NaBr溶液、KI溶液、AgNO3溶液,该试剂是( )| A. | 氯水 | B. | H2O | C. | 稀盐酸 | D. | NaOH溶液 |
分析 NaCl溶液、NaBr溶液、KI溶液、AgNO3溶液分别与氯水混合的现象为:无现象、橙色溶液、紫色溶液、白色沉淀,以此来解答.
解答 解:分别与氯水混合,无现象的为NaCl,橙色溶液的为NaBr、紫色溶液的为NaI,白色沉淀生成的为AgNO3溶液,可鉴别,故A选;
B.均与水不反应,现象相同,不能鉴别,故B不选;
C.稀盐酸不能鉴别NaCl溶液、NaBr溶液、KI溶液,故C不选;
D.NaOH溶液不能鉴别NaCl溶液、NaBr溶液、KI溶液,故D不选;
故选A.
点评 本题考查物质的鉴别,为高频考点,把握物质的性质、发生的反应及现象为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.2014年5月3日,科学家在粒子加速器中,用钙离子轰击放射性元素锫,成功生成117号元素,有关该元素的说法正确的是( )
| A. | 117号元素位于第七周期第ⅦB族 | B. | 117号元素是一种金属元素 | ||
| C. | 117号元素最外层有5个电子 | D. | 117号元素没有正化合价 |
20.下列说法中不正确的是( )
| A. | 若XY3分子中X原子处于正三角形的中心,则XY3分子为非极性分子 | |
| B. | C2H5OH与C2H5Br相比,前者的沸点远高于后者,其原因是前者的分子间存在氢键 | |
| C. | 同周期ⅠA族元素和ⅦA族元素之间只能形成离子化合物 | |
| D. | 由两种非金属元素组成的化合物分子中只可能有极性键,不会有非极性键 |
17.石材的放射性常用镭(${\;}_{88}^{226}$Ra)作为标准,居里夫人(Marie Curie)因对Ra元素的研究曾两度获得诺贝尔奖.下列有关镭(${\;}_{88}^{226}$Ra)的叙述中不正确的是( )
| A. | ${\;}_{88}^{226}$Ra原子核内有138个中子 | B. | ${\;}_{88}^{226}$Ra原子核外有88个电子 | ||
| C. | ${\;}_{88}^{226}$Ra原子核内有88个质子 | D. | Ra元素位于第六周期 |
4.现有部分短周期元素的原子结构如下表:
(1)写出X的元素符号:N,Z元素原子的质量数为23.
(2)元素Y的最高价氧化物的结构式为O=C=O,Z元素的单质在空气中燃烧产物的电子式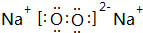 ,用电子式表示X的气态氢化物的形成过程
,用电子式表示X的气态氢化物的形成过程 .
.
(3)Y的最高价氧化物和Z元素的单质在空气中燃烧产物发生反应的化学方程式为2CO2+2Na2O2=2Na2CO3+O2;若反应过程中,转移电子数为6.02×1023,则消耗Y的最高价氧化物的质量为1mol.
| 元素 编号 | 元素原子结构 |
| X | 原子结构示意图为 |
| Y | 最外层电子数是次外层电子数的2倍 |
| Z | 原子核内含有12个中子,且其离子的结构示意图为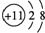 |
(2)元素Y的最高价氧化物的结构式为O=C=O,Z元素的单质在空气中燃烧产物的电子式
 ,用电子式表示X的气态氢化物的形成过程
,用电子式表示X的气态氢化物的形成过程 .
.(3)Y的最高价氧化物和Z元素的单质在空气中燃烧产物发生反应的化学方程式为2CO2+2Na2O2=2Na2CO3+O2;若反应过程中,转移电子数为6.02×1023,则消耗Y的最高价氧化物的质量为1mol.
14.某气体有机物在氧气中燃烧生成二氧化碳和水的实验事实说明( )
| A. | 该有机物的分子式为CH4 | B. | 该有机物中含碳元素和氢元素 | ||
| C. | 该有机物中只含有碳元素和氢元素 | D. | 该有机物的化学性质比较稳定 |
1.下列关于碱金属的描述正确的是( )
| A. | 碱金属都可以保存在煤油中 | |
| B. | 碱金属元素的单质硬度小、密度小、熔点低 | |
| C. | 在空气中加热均可生成多种氧化物 | |
| D. | 碱金属与水反应,均漂浮在水面上 |
18.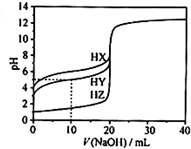 25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法不正确的是( )
25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法不正确的是( )
 25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法不正确的是( )
25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL浓度均为0.1000mol/L的三种酸HX、HY、HZ,滴定曲线如图所示.下列说法不正确的是( )| A. | 在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ>HY>HX | |
| B. | 根据滴定曲线,可得Ka(HY)≈10-5 | |
| C. | 将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(Y-)>c(X-)>c(OH-)>c(H+) | |
| D. | HY与HZ混合,达到平衡时:c(H+)=$\frac{{k}_{2}(HY)•c(HY)}{c({Y}^{-})}$+c(Z-)+c(OH-) |
19.下列叙述中正确的是( )
| A. | 发生化学反应时,失去电子越多的金属原子,其还原能力越强 | |
| B. | 目前已发现118种元素,即已发现118种原子 | |
| C. | 核外电子总数相同的粒子,必定是同种元素的原子 | |
| D. | 同一元素的各种同位素的化学性质基本相同 |