题目内容
下列说法不正确的是( )
| A、电镀过程中电镀液溶质的浓度基本保持不变 |
| B、弱电解质溶液可能比强电解溶液导电能力强 |
| C、使用催化剂可以降低反应的活化能 |
| D、使用催化剂可以使反应的平衡常数增大 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.电镀时,阳极上溶解金属的质量基本等于阴极析出金属的质量;
B.溶液导电能力与离子浓度成正比,与电解质强弱无关;
C.催化剂可以降低反应的活化能,从而改变反应速率;
D.化学平衡常数只与温度有关,与其它条件无关.
B.溶液导电能力与离子浓度成正比,与电解质强弱无关;
C.催化剂可以降低反应的活化能,从而改变反应速率;
D.化学平衡常数只与温度有关,与其它条件无关.
解答:
解:A.电镀时,阳极上溶解金属的质量基本等于阴极析出金属的质量,所以电镀过程中电镀液溶质的浓度基本保持不变,故A正确;
B.溶液导电能力与离子浓度成正比,与电解质强弱无关,所以弱电解质溶液可能比强电解溶液导电能力强,故B正确;
C.使用催化剂,可改变反应历程,降低活化能,故C正确;
D.化学平衡常数只与温度有关,温度不变,则化学平衡常数不变,催化剂能同等程度的改变正逆反应速率,不影响平衡常数,故D错误;
故选D.
B.溶液导电能力与离子浓度成正比,与电解质强弱无关,所以弱电解质溶液可能比强电解溶液导电能力强,故B正确;
C.使用催化剂,可改变反应历程,降低活化能,故C正确;
D.化学平衡常数只与温度有关,温度不变,则化学平衡常数不变,催化剂能同等程度的改变正逆反应速率,不影响平衡常数,故D错误;
故选D.
点评:本题考查较综合,涉及电解原理、催化剂的作用、平衡常数的影响因素、溶液导电能力的影响因素,易错选项是B,溶液导电能力与离子浓度、离子多带电荷有关,与电解质强弱无关.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
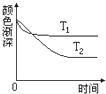 反应:A+B?2C,其中A为有色气体,其混合物颜色深浅与反应时间、温度(T)之间的关系如图所示(B、C均为无色物质).下列说法中不正确的是( )
反应:A+B?2C,其中A为有色气体,其混合物颜色深浅与反应时间、温度(T)之间的关系如图所示(B、C均为无色物质).下列说法中不正确的是( )| A、T1>T2,该反应是放热反应 |
| B、若A、B、C均为气态物质,增大压强时B的转化率不变 |
| C、若A、B、C均为气态物质时,增大压强,混合气体的颜色不变 |
| D、若A、B为气体,C为固体,增大压强时A的转化率增大 |
2012年3月22日是第二十届“世界水日”,3月22-28日是第二十五届“中国水周”. 联合国确定今年“世界水日”的宣传主题是“水与粮食安全”( Water and Food Security).下列跟水有关的变化中没有化学变化的是( )
| A、海水晒盐 |
| B、太阳能光解水制氢气 |
| C、饮用水生产 |
| D、肥皂水区分硬水和软水 |
“神舟”五号载人飞船发射成功后,我国又在启动“嫦娥工程”,在3-4年内中国人登上月球.人类探测月球发现,其土壤中存在较丰富的质量数为3的氦,它可以作为核聚变的重要原料之一.以下叙述正确的是( )
| A、由质量数为3的氦原子构成的分子是双原子分子 |
| B、23He与24He的性质均相同 |
| C、23He中的质子数与24He的中子数相等 |
| D、23He、24He 形成的分子中存在共价键 |
在实验室里,要想使AlCl3中的Al3+全部沉淀出来,应选用下列试剂中的( )
| A、石灰水 | B、氢氧化钠溶液 |
| C、硫酸 | D、氨水 |
下列溶液与铝不能发生反应产生氢气的是( )
| A、盐酸溶液 |
| B、氢氧化钠溶液 |
| C、氯化铵溶液 |
| D、硫酸钠溶液 |
某可逆反应a A(g)+bB(g)?cC(g),在温度分别为T1和T2,压强分别为P1和P2条件下,得到C的物质的量n与时间t的关系曲线如下图所示.据图分析,以下正确的是( )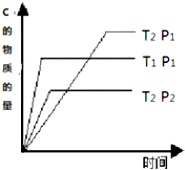

| A、c>a+b,正反应为吸热反应 |
| B、c>a+b,正反应为放热反应 |
| C、c<a+b,逆反应为吸热反应 |
| D、c<a+b,逆反应为放热反应 |
下列各组物质中,无论以任何比例混合,其密度不变的是( )
| A、CO与C2H4 |
| B、C2H6与C2H4 |
| C、CO2与C3H6 |
| D、CH4与C2H4 |
下列分子式①C2H6O ②C4H10 ③N2 ④C ⑤CH4 ⑥P,表示的物质一定是纯净物的是( )
| A、③⑤⑥ | B、③⑤ |
| C、③④⑤⑥ | D、②③④⑤⑥ |