题目内容
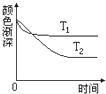 反应:A+B?2C,其中A为有色气体,其混合物颜色深浅与反应时间、温度(T)之间的关系如图所示(B、C均为无色物质).下列说法中不正确的是( )
反应:A+B?2C,其中A为有色气体,其混合物颜色深浅与反应时间、温度(T)之间的关系如图所示(B、C均为无色物质).下列说法中不正确的是( )| A、T1>T2,该反应是放热反应 |
| B、若A、B、C均为气态物质,增大压强时B的转化率不变 |
| C、若A、B、C均为气态物质时,增大压强,混合气体的颜色不变 |
| D、若A、B为气体,C为固体,增大压强时A的转化率增大 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、依据先拐先平温度高,结合化学平衡移动原理分析判断反应热量变化;
B、若A、B、C均为气态物质,反应前后气体体积不变,改变压强平衡不动;
C、若A、B、C均为气态物质时,增大压强,浓度增大混合气体的颜色变深;
D、若A、B为气体,C为固体,增大压强时,平衡正向进行;
B、若A、B、C均为气态物质,反应前后气体体积不变,改变压强平衡不动;
C、若A、B、C均为气态物质时,增大压强,浓度增大混合气体的颜色变深;
D、若A、B为气体,C为固体,增大压强时,平衡正向进行;
解答:
解:A、依据先拐先平温度高,T1>T2,温度越高,气体颜色越深,说明平衡逆向进行,所以正反应为放热反应,故A正确;
B、若A、B、C均为气态物质,反应前后气体体积不变,改变压强平衡不动,B的转化率不变,故B正确;
C、若A、B、C均为气态物质时,增大压强,浓度增大混合气体的颜色变深,故错误;
D、若A、B为气体,C为固体,增大压强时,平衡正向进行,A的转化率增大,故D正确;
故选C.
B、若A、B、C均为气态物质,反应前后气体体积不变,改变压强平衡不动,B的转化率不变,故B正确;
C、若A、B、C均为气态物质时,增大压强,浓度增大混合气体的颜色变深,故错误;
D、若A、B为气体,C为固体,增大压强时,平衡正向进行,A的转化率增大,故D正确;
故选C.
点评:本题考查了化学平衡影响因素分析判断,化学平衡移动原理和反应特征是解题关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列离子方程式中,不正确的是( )
| A、KI的酸性溶液长期置于空气中:4I-+4H++O2═2I2+2H2O |
| B、高锰酸钾酸性溶液与草酸溶液反应:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O |
| C、用稀硫酸除去铁片表面的铁锈:FeO+2H+═Fe2++H2O |
| D、硫代硫酸钠溶液中滴加稀硫酸:2H++S2O32-═S↓+SO2↑+H2O |
在通常条件下,下列性质排列正确的是( )
| A、熔点:MgO>KCl>SiO2>CO2 |
| B、水中溶解性:HCl>NH3>H2S>SO3 |
| C、热稳定性:HF>H2O>NH3 |
| D、沸点:戊烷>2-甲基丁烷>乙烷>丁烷 |
已知反应:
①Cl2+2KBr=2KCl+Br2,
②KClO3+6HCl=3Cl2↑+KCl+3H2O,
③2KBrO3+Cl2=Br2+2KClO3,
下列说法正确的是( )
①Cl2+2KBr=2KCl+Br2,
②KClO3+6HCl=3Cl2↑+KCl+3H2O,
③2KBrO3+Cl2=Br2+2KClO3,
下列说法正确的是( )
| A、上述三个反应都有单质生成,所以都是置换反应 |
| B、反应③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol |
| C、反应②中还原剂与氧化剂的物质的量之比为6:1 |
| D、氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2 |
在标准状况下,2.2g由CH4和C2H4组成的混合气体所占的体积为2.24L,则该混合气体中CH4和C2H4的质量比是( )
| A、1:1 | B、4:7 |
| C、7:4 | D、1:2 |
下列关于蛋白质的叙述中,不正确的是( )
| A、向蛋白质溶液里加(NH4)2SO4溶液可提纯蛋白质 |
| B、在豆浆中加入少量的石膏,能使豆浆凝结为豆腐 |
| C、温度越高,酶对某些化学反应的催化效率越高 |
| D、当人误食重金属盐类时,可以喝大量的牛奶、蛋清解毒 |
下列说法不正确的是( )
| A、电镀过程中电镀液溶质的浓度基本保持不变 |
| B、弱电解质溶液可能比强电解溶液导电能力强 |
| C、使用催化剂可以降低反应的活化能 |
| D、使用催化剂可以使反应的平衡常数增大 |
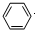 +CH2=CH2
+CH2=CH2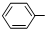 CH2CH2
CH2CH2