题目内容
已知:

Ⅰ制备1-溴丁烷粗产品
(1)在如图1装置的圆底烧瓶中依次加入NaBr,10mL正丁醇,2粒沸石,分批加入1:1的硫酸溶液,摇匀,加热30min.写出制备1-溴丁烷的化学反应方程式: .
(2)①图1反应装置中加入沸石的目的是 ;
②配制体积比为1:1的硫酸所用的定量仪器为 (选填编号).
a.天平 b.量筒 c.容量瓶 d.滴定管
(3)图1反应装置中,除了产物和水之外,还可能存在 等有机副产物.
(4)若用浓硫酸进行实验,有机层中会呈现棕黄色,除去其中杂质的正确方法是 (选填编号).
a蒸馏 b氢氧化钠溶液 c用四氯化碳萃取 d用亚硫酸钠溶液洗涤
Ⅱ制备精品
(5)将得到的粗1-溴丁烷依次用浓硫酸、水、10%碳酸钠,水洗涤后,加入无水氯化钙进行干燥,然后再将1-溴丁烷按如图2装置蒸馏.收集产品时,控制的温度应在 ℃;区分溴丁烷精品和粗品的一种方法是 .
(6)实验制得的溴丁烷的质量为10.895g,则正丁醇的转化率为 .(保留3位小数)
| 药品名称 | 熔点/℃ | 沸点(℃) | 密度 g/cm3 | 溶解性 |
| 正丁醇 | -89.5 | 117.7 | 0.8098 | 微溶于水、溶于浓硫酸 |
| 1-溴丁烷 | -112.4 | 101.6 | 1.2760 | 不溶于水和浓硫酸 |

Ⅰ制备1-溴丁烷粗产品
(1)在如图1装置的圆底烧瓶中依次加入NaBr,10mL正丁醇,2粒沸石,分批加入1:1的硫酸溶液,摇匀,加热30min.写出制备1-溴丁烷的化学反应方程式:
(2)①图1反应装置中加入沸石的目的是
②配制体积比为1:1的硫酸所用的定量仪器为
a.天平 b.量筒 c.容量瓶 d.滴定管
(3)图1反应装置中,除了产物和水之外,还可能存在
(4)若用浓硫酸进行实验,有机层中会呈现棕黄色,除去其中杂质的正确方法是
a蒸馏 b氢氧化钠溶液 c用四氯化碳萃取 d用亚硫酸钠溶液洗涤
Ⅱ制备精品
(5)将得到的粗1-溴丁烷依次用浓硫酸、水、10%碳酸钠,水洗涤后,加入无水氯化钙进行干燥,然后再将1-溴丁烷按如图2装置蒸馏.收集产品时,控制的温度应在
(6)实验制得的溴丁烷的质量为10.895g,则正丁醇的转化率为
考点:制备实验方案的设计
专题:实验题
分析:(1)醇和氢卤酸能在加热条件下发生取代反应生成卤代烃,故制备1-溴丁烷的化学反应方程式可以看成是正丁醇中羟基被溴原子取代即:NaBr+H2SO4+CH3CH2CH2CH2OH→CH3CH2CH2CH2Br+NaHSO4+H2O;
(2)反应装置中加入沸石的目的是防止暴沸;用量筒量取相同量的硫酸和水进行混合,故定量仪器为b.量筒;
(3)醇在浓硫酸并加热条件下还会发生消去反应和分子间脱水生成醚的反应,故还可能存1-丁烯,丁醚等有机副产物;
(4)若用浓硫酸进行实验,由于浓硫酸具有强氧化性会使部分溴离子氧化为溴单质;a中蒸馏也会使部分原料物挥发出来,达不到效果;b中氢氧化钠溶液洗涤,会使卤代烃发生水解造成损失; c中用四氯化碳无法萃取,由于溴和卤代烃都能溶于四氯化碳;d中用亚硫酸钠溶液洗涤可和溴发生氧化还原反应,再通过分液操作即可分离;
(5)根据表中1-溴丁烷的沸点可知收集产品时,控制的温度应在101.6℃左右; 区分1-溴丁烷精品和粗品的一种方法是可通过测熔沸点;
(6)由方程式NaBr+H2SO4+CH3CH2CH2CH2OH→CH3CH2CH2CH2Br+NaHSO4+H2O;制得的1-溴丁烷的质量为10.895 g,求则正丁醇的质量,再用此质量除以0.8098*10,求出转化率为0.727.
(2)反应装置中加入沸石的目的是防止暴沸;用量筒量取相同量的硫酸和水进行混合,故定量仪器为b.量筒;
(3)醇在浓硫酸并加热条件下还会发生消去反应和分子间脱水生成醚的反应,故还可能存1-丁烯,丁醚等有机副产物;
(4)若用浓硫酸进行实验,由于浓硫酸具有强氧化性会使部分溴离子氧化为溴单质;a中蒸馏也会使部分原料物挥发出来,达不到效果;b中氢氧化钠溶液洗涤,会使卤代烃发生水解造成损失; c中用四氯化碳无法萃取,由于溴和卤代烃都能溶于四氯化碳;d中用亚硫酸钠溶液洗涤可和溴发生氧化还原反应,再通过分液操作即可分离;
(5)根据表中1-溴丁烷的沸点可知收集产品时,控制的温度应在101.6℃左右; 区分1-溴丁烷精品和粗品的一种方法是可通过测熔沸点;
(6)由方程式NaBr+H2SO4+CH3CH2CH2CH2OH→CH3CH2CH2CH2Br+NaHSO4+H2O;制得的1-溴丁烷的质量为10.895 g,求则正丁醇的质量,再用此质量除以0.8098*10,求出转化率为0.727.
解答:
解:(1)醇和氢卤酸能在加热条件下发生取代反应生成卤代烃,故制备1-溴丁烷的化学反应方程式可以看成是正丁醇中羟基被溴原子取代即:NaBr+H2SO4+CH3CH2CH2CH2OH→CH3CH2CH2CH2Br+NaHSO4+H2O;
故答案为:NaBr+H2SO4+CH3CH2CH2CH2OH→CH3CH2CH2CH2Br+NaHSO4+H2O;
(2)反应装置中加入沸石的目的是防止暴沸;用量筒量取相同量的硫酸和水进行混合,故定量仪器为b.量筒;
故答案为:防止暴沸;b;
(3)醇在浓硫酸并加热条件下还会发生消去反应和分子间脱水生成醚的反应,故还可能存1-丁烯,丁醚等有机副产物;
故答案为:1-丁烯、丁醚;
(4)若用浓硫酸进行实验,由于浓硫酸具有强氧化性会使部分溴离子氧化为溴单质;
a中蒸馏也会使部分原料物挥发出来,达不到效果.;
b中氢氧化钠溶液洗涤,会使卤代烃发生水解造成损失;
c中用四氯化碳无法萃取,由于溴和卤代烃都能溶于四氯化碳;
d中用亚硫酸钠溶液洗涤可和溴发生氧化还原反应,再通过分液操作即可分离;
故答案为:d;
(5)根据表中1-溴丁烷的沸点可知收集产品时,控制的温度应在101.6℃左右; 区分1-溴丁烷精品和粗品的一种方法是可通过测熔沸点;
故答案为:101.6;测熔沸点;
(6)由方程式NaBr+H2SO4+CH3CH2CH2CH2OH→CH3CH2CH2CH2Br+NaHSO4+H2O.制得的1-溴丁烷的质量为10.895 g,求则正丁醇的质量,再用此质量除以0.8098*10,求出转化率为0.727;
故答案为:0.727.
故答案为:NaBr+H2SO4+CH3CH2CH2CH2OH→CH3CH2CH2CH2Br+NaHSO4+H2O;
(2)反应装置中加入沸石的目的是防止暴沸;用量筒量取相同量的硫酸和水进行混合,故定量仪器为b.量筒;
故答案为:防止暴沸;b;
(3)醇在浓硫酸并加热条件下还会发生消去反应和分子间脱水生成醚的反应,故还可能存1-丁烯,丁醚等有机副产物;
故答案为:1-丁烯、丁醚;
(4)若用浓硫酸进行实验,由于浓硫酸具有强氧化性会使部分溴离子氧化为溴单质;
a中蒸馏也会使部分原料物挥发出来,达不到效果.;
b中氢氧化钠溶液洗涤,会使卤代烃发生水解造成损失;
c中用四氯化碳无法萃取,由于溴和卤代烃都能溶于四氯化碳;
d中用亚硫酸钠溶液洗涤可和溴发生氧化还原反应,再通过分液操作即可分离;
故答案为:d;
(5)根据表中1-溴丁烷的沸点可知收集产品时,控制的温度应在101.6℃左右; 区分1-溴丁烷精品和粗品的一种方法是可通过测熔沸点;
故答案为:101.6;测熔沸点;
(6)由方程式NaBr+H2SO4+CH3CH2CH2CH2OH→CH3CH2CH2CH2Br+NaHSO4+H2O.制得的1-溴丁烷的质量为10.895 g,求则正丁醇的质量,再用此质量除以0.8098*10,求出转化率为0.727;
故答案为:0.727.
点评:本题主要考查对物质的分离,离子的检验,粗盐的提纯 等考点的理解,难度不大.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
由一种阳离子与两种酸根离子组成的盐称为混盐.混盐CaOC12在酸性条件下可以产生C12,下列关于混盐CaOC12的有关判断不正确的是( )
| A、该混盐与硫酸反应产生1molC12时转移2NA个电子 |
| B、该混盐的水溶液呈碱性 |
| C、该混盐具有较强的氧化性 |
| D、该混盐中氯元素的化合价为+1和-1 |
下列化学用语能正确表示相应意义的是( )
| A、乙烯的结构简式C2H4 |
| B、丁烷的结构简式CH3(CH2)2CH3 |
C、四氯化碳的结构式 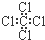 |
D、苯的分子式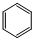 |
药物贝诺酯可由乙酰水杨酸和对乙酰氨其酚在一定条件下反应制得:
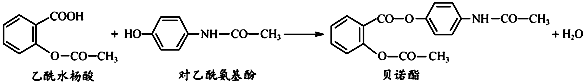
下列有关叙述正确的是( )

下列有关叙述正确的是( )
| A、1mol贝诺酯分子可与9mol H2完全反应 |
| B、可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚 |
| C、贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠 |
| D、乙酰水杨酸和乙酰氨基酚均可与NaHCO3溶液反应 |
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:下列说法错误的是( )
| 物质 | X | Y | Z |
| 初始浓度/mol/L | 1 | 2 | 0 |
| 平衡浓度/mol/L | 0.6 | 1.6 | 0.8 |
| A、增大压强使平衡向生成Z的方向移动,平衡常数增大 | ||
B、反应可表示为X+Y?2Z,其平衡常数为
| ||
| C、反应达到平衡时,Y的转化率为20% | ||
| D、改变温度可以改变此反应的平衡常数 |
若以M表示氮气的摩尔质量,V表示在标准状况下氮气的摩尔体积,ρ为在标准状况下氮气的密度,NA为阿伏加德罗常数,m、△分别表示每个氮气分子的质量和体积,下面是四个关系式:①NA=
,②ρ=
,③m=
,④△=
,其中正确的个数( )
| Vρ |
| M |
| M |
| NA△ |
| M |
| NA |
| V |
| NA |
| A、4个 | B、3 个 |
| C、2个 | D、1个 |
KCl中有少量的KI,为了除去杂质,可选用以下操作中的( )
①加入碘水 ②通入Cl2 ③用CCl4萃取 ④过滤.
①加入碘水 ②通入Cl2 ③用CCl4萃取 ④过滤.
| A、①③ | B、①④ | C、②③ | D、②④ |
