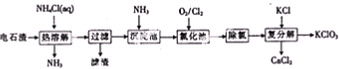
题目内容
KCl中有少量的KI,为了除去杂质,可选用以下操作中的( )
①加入碘水 ②通入Cl2 ③用CCl4萃取 ④过滤.
①加入碘水 ②通入Cl2 ③用CCl4萃取 ④过滤.
| A、①③ | B、①④ | C、②③ | D、②④ |
考点:物质的分离、提纯和除杂,氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:除杂时不能引入新的杂质,更不能影响被提纯的物质的性质.通入氯气使KI氧化成碘单质,同时氯气被还原成氯离子.
解答:
解:除杂时不能引入新的杂质,更不能影响被提纯的物质的性质.通入氯气使KI氧化成碘单质,同时氯气被还原成氯离子.反应的化学方程式为Cl2+KI=KCl+I2,离子方程式为Cl2+I-=Cl-+I2;然后用CCl4萃取;
故选C.
故选C.
点评:本题考查物质的分离和提纯,难度不大,注意把握物质的性质异同,除杂时不能引入新的杂质,更不能影响被提纯的物质的性质.

练习册系列答案
相关题目
下列仪器使用前必须检查其是否漏水的是( )
①分液漏斗 ②蒸馏烧瓶 ③冷凝管 ④容量瓶 ⑤蒸发皿 ⑥长颈漏斗.
①分液漏斗 ②蒸馏烧瓶 ③冷凝管 ④容量瓶 ⑤蒸发皿 ⑥长颈漏斗.
| A、②⑥ | B、①④ | C、③④ | D、③⑤ |
用分液漏斗可以分离的一组液体混合物是( )
| A、硝基苯和水 | B、溴和四氯化碳 |
| C、苯和溴苯 | D、己烷和苯 |
在元素周期表中,金属元素与非金属元素分界线附近,能找到( )
| A、制半导体材料的元素 |
| B、制农药的元素 |
| C、制催化剂的元素 |
| D、制耐高温合金的元素 |
下列说法正确的是(NA代表着阿伏加德罗常数的值)( )
| A、1molNa被完全氧化为Na2O2,失去的电子数为2NA |
| B、常温常压下,16gO3气体含有氧原子数为NA |
| C、常温常压下,22.4LCO2 含有分子数为NA |
| D、18g D2O所含有电子数为10NA |
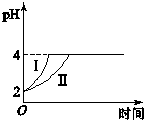 在常温下,取pH=2的盐酸和醋酸溶液各100mL.向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图( )
在常温下,取pH=2的盐酸和醋酸溶液各100mL.向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图( )| A、曲线Ⅰ表示盐酸的pH变化 |
| B、曲线Ⅱ表示盐酸的pH变化 |
| C、在相同条件下,两溶液生成的气体体积相等 |
| D、醋酸溶液中加入锌的质量比盐酸溶液中多 |

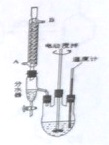 邻苯二甲酸二异癸酯为无色粘稠液体,密度约为0.966g?cm-3,不溶于水,易溶于有机溶剂,常用作耐热塑料增塑剂,某实验小组用如图所示装置制取少量邻苯二甲酸二异癸酯(图中夹持和加热装置已略去).主要操作步骤如下:
邻苯二甲酸二异癸酯为无色粘稠液体,密度约为0.966g?cm-3,不溶于水,易溶于有机溶剂,常用作耐热塑料增塑剂,某实验小组用如图所示装置制取少量邻苯二甲酸二异癸酯(图中夹持和加热装置已略去).主要操作步骤如下: