题目内容
将下列物质进行分类
(1)Fe(OH)3(2)SO2(4)HCl(5)盐酸(6)硫酸 (7)氨气 (9)一水合氨NH3?H2O(10)氨水 (11)熔融的氯化钠 (13)铜粉 (14)CuSO4溶液
电解质: ,非电解质 ,强电解质 ,弱电解质 .
(1)Fe(OH)3(2)SO2(4)HCl(5)盐酸(6)硫酸 (7)氨气 (9)一水合氨NH3?H2O(10)氨水 (11)熔融的氯化钠 (13)铜粉 (14)CuSO4溶液
电解质:
考点:电解质与非电解质,强电解质和弱电解质的概念
专题:离子反应专题
分析:电解质:在水溶液中或熔融状态下能够导电的化合物;
非电解质:在熔融状态和水溶液中都不能导电的化合物;在水溶液中完全电离的是强电解质;部分电离的是弱电解质.
非电解质:在熔融状态和水溶液中都不能导电的化合物;在水溶液中完全电离的是强电解质;部分电离的是弱电解质.
解答:
解:(1)Fe(OH)3在水溶液中部分电离,是弱电解质,
(2)SO2自身不能电离,是非电解质,
(4)HCl溶于水完全电离,是强电解质,
(5)盐酸是混合物,既不是电解质也不是非电解质,
(6)硫酸溶于水完全电离,是强电解质,
(7)NH3自身不能电离,是非电解质,
(9)一水合氨NH3?H2O在水溶液中部分电离,是弱电解质,
(10)氨水是混合物,既不是电解质也不是非电解质;
(11)熔融的氯化钠溶于水完全电离,是强电解质,
(13)铜粉为金属单质,既不是电解质也不是非电解质;
(14)CuSO4溶液是混合物,既不是电解质也不是非电解质;
故属于电解质的是:(1)(4)(6)(9)(11);属于非电解质的是:(2)(7);属于强电解质的是:(4)(6)(11);属于弱电解质的是:(1)(9),
故答案为:(1)(4)(6)(9)(11);(2)(7);(4)(6)(11);(1)(9).
(2)SO2自身不能电离,是非电解质,
(4)HCl溶于水完全电离,是强电解质,
(5)盐酸是混合物,既不是电解质也不是非电解质,
(6)硫酸溶于水完全电离,是强电解质,
(7)NH3自身不能电离,是非电解质,
(9)一水合氨NH3?H2O在水溶液中部分电离,是弱电解质,
(10)氨水是混合物,既不是电解质也不是非电解质;
(11)熔融的氯化钠溶于水完全电离,是强电解质,
(13)铜粉为金属单质,既不是电解质也不是非电解质;
(14)CuSO4溶液是混合物,既不是电解质也不是非电解质;
故属于电解质的是:(1)(4)(6)(9)(11);属于非电解质的是:(2)(7);属于强电解质的是:(4)(6)(11);属于弱电解质的是:(1)(9),
故答案为:(1)(4)(6)(9)(11);(2)(7);(4)(6)(11);(1)(9).
点评:本题重点考查电解质、非电解质、强弱电解质概念的辨析,难度不大.要注意在水溶液中完全电离的是强电解质;部分电离的是弱电解质.

练习册系列答案
相关题目
取一定量的NH4NO3和(NH4)2SO4固体混合物,分成质量相等的两等份.一份与足量的NaOH浓溶液共热,在标准状况下收集到6.72L NH3;另一份加水完全溶解后,加入过量的BaCl2溶液得到11.65g白色沉淀.下列说法错误的是( )
| A、原固体混合中n[(NH4)2SO4]=0.05 mol |
| B、原固体混合中m(NH4NO3)=16 g |
| C、若完全溶解后溶液的体积为100 mL,则c(NH4NO3)=4 mol?L-1 |
| D、原固体混合中n(NH4NO3):n[(NH4)2SO4]=4:1 |
已知NaHCO3在150℃下会发生分解反应:2NaHCO3
Na2CO3+CO2↑+H2O,则反应生成的混合气体对氢气的相对密度是( )
| ||
| A、15.5 | B、42 |
| C、31 | D、21 |
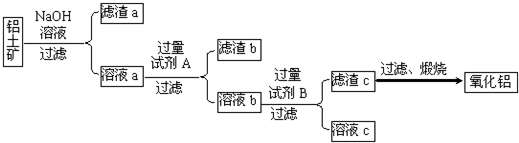
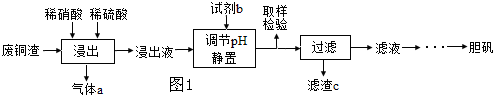
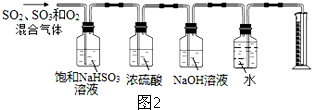
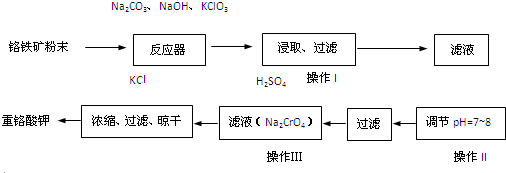
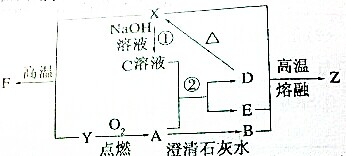 已知下列物质有如图所示转化关系,水和部分产物已略去.
已知下列物质有如图所示转化关系,水和部分产物已略去.