题目内容
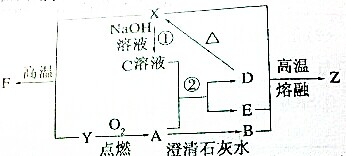 已知下列物质有如图所示转化关系,水和部分产物已略去.
已知下列物质有如图所示转化关系,水和部分产物已略去.①X为不溶于水的坚硬固体,Z无固定熔点,是现代建筑中不可缺少的装饰材料;
②无色气体A是引起温室效应的主要气体;
③B、D均为难溶于水的白色固体;
④高纯度的F是制造电脑芯片的一种非金属单质.
据此回答下列问题:
(1)B的化学式是
(2)由X、Y制F的过程中,Y作
(3)转化①的化学方程式为
(4)转化②(A少量)的离子方程式为
考点:无机物的推断
专题:推断题
分析:①X为不溶于水的坚硬固体,Z无固定熔点,是现代建筑中不可缺少的装饰材料,判断为玻璃,说明X为SiO2;
②无色气体A是引起温室效应的主要气体为CO2;
③B、D均为难溶于水的白色固体,流程分析可知B为CaCO3,;
④高纯度的F是制造电脑芯片的一种非金属单质为SiO2;
结合流程分析判断可知X为SiO2,B为CaCO3,C为Na2SiO3,D为H2SiO3,E为Na2CO3,Z为玻璃,Y为CO,F为Si.
②无色气体A是引起温室效应的主要气体为CO2;
③B、D均为难溶于水的白色固体,流程分析可知B为CaCO3,;
④高纯度的F是制造电脑芯片的一种非金属单质为SiO2;
结合流程分析判断可知X为SiO2,B为CaCO3,C为Na2SiO3,D为H2SiO3,E为Na2CO3,Z为玻璃,Y为CO,F为Si.
解答:
解:①X为不溶于水的坚硬固体,Z无固定熔点,是现代建筑中不可缺少的装饰材料,判断为玻璃,说明X为SiO2;
②无色气体A是引起温室效应的主要气体为CO2;
③B、D均为难溶于水的白色固体,流程分析可知B为CaCO3,;
④高纯度的F是制造电脑芯片的一种非金属单质为SiO2;
结合流程分析判断可知X为SiO2,B为CaCO3,C为Na2SiO3,D为H2SiO3,E为Na2CO3,Z为玻璃,Y为CO,F为Si;
(1)B的化学式是CaCO3,F的名称是粗硅,故答案为:CaCO3;粗硅;
(2)由X、Y制F的过程为SiO2+2CO
2CO2+Si,CO做还原剂,故答案为:还原;
(3)转化①的化学方程式为:SiO2+2NaOH=Na2SiO3+H2O;
故答案为:SiO2+2NaOH=Na2SiO3+H2O;
(4)转化②(A少量)的反应是二氧化碳和硅酸钠发生的反应生成硅酸沉淀和碳酸钠,反应的离子方程式为:CO2+SiO32-+H2O=H2SiO3↓+CO32-;
故答案为:CO2+SiO32-+H2O=H2SiO3↓+CO32-.
②无色气体A是引起温室效应的主要气体为CO2;
③B、D均为难溶于水的白色固体,流程分析可知B为CaCO3,;
④高纯度的F是制造电脑芯片的一种非金属单质为SiO2;
结合流程分析判断可知X为SiO2,B为CaCO3,C为Na2SiO3,D为H2SiO3,E为Na2CO3,Z为玻璃,Y为CO,F为Si;
(1)B的化学式是CaCO3,F的名称是粗硅,故答案为:CaCO3;粗硅;
(2)由X、Y制F的过程为SiO2+2CO
| ||
(3)转化①的化学方程式为:SiO2+2NaOH=Na2SiO3+H2O;
故答案为:SiO2+2NaOH=Na2SiO3+H2O;
(4)转化②(A少量)的反应是二氧化碳和硅酸钠发生的反应生成硅酸沉淀和碳酸钠,反应的离子方程式为:CO2+SiO32-+H2O=H2SiO3↓+CO32-;
故答案为:CO2+SiO32-+H2O=H2SiO3↓+CO32-.
点评:本题考查了物质转化关系分析判断,物质性质的理解应用,主要是碳、硅及其化合物性质的应用,掌握基础是关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
两种金属粉末混合物14克,投入足量的稀硫酸中,产生1克氢气,则金属的混合物不可能是( )
①Fe ②Zn ③Al ④Mg.
①Fe ②Zn ③Al ④Mg.
| A、①② | B、②③ | C、①③ | D、①④ |
生活中碰到的某些问题,常涉及到化学知识,下列说法不正确的是( )
| A、鱼虾放久了会产生不愉快的腥臭气味,应当用水冲洗,并在烹调时加人少量食醋 |
| B、“酸可除锈”“洗涤剂可去油”都是发生了化学变化 |
| C、被蜂蚁蜇咬会感到疼痛难忍,这是蜂蚁咬人时将甲酸注人人体的缘故,此时若能涂抹稀氨水或碳酸氢钠溶液,可以减轻疼痛 |
| D、食品包装袋中常放入小袋的生石灰,目的是防止食品潮解变质 |
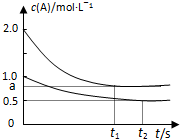 向甲、乙两恒温恒容的密闭容器中,分别充入一定量的A和B,发生反应:A(g)+B(g)?xC(g)△H<0.测得两容器中c(A)随时间t的变化如图所示:下列说法正确的是( )
向甲、乙两恒温恒容的密闭容器中,分别充入一定量的A和B,发生反应:A(g)+B(g)?xC(g)△H<0.测得两容器中c(A)随时间t的变化如图所示:下列说法正确的是( ) | 容器 | 甲 | 乙 |
| 容积(L) | 0.5 | 0.5 |
| 反应放热(kJ) | Q1 | Q2 |
| 反应物起始量 | 1 molA 1 molB | 0.5 molA 0.5 molB |
| A、x=1 |
| B、Q1<2Q2 |
| C、根据题中信息无法计算a值 |
| D、保持其他条件不变,起始时向乙容器充入0.2 mol A、0.2 mol B、0.2 mol C,则此时v(正)<v(逆) |
向混浊的水中加入明矾〔K Al (SO4)2?12H2O〕后,水可得到净化,其中起到净化作用的是( )
| A、k+ |
| B、Al3+ |
| C、SO42- |
| D、明矾溶于水后产生的氢氧化铝胶体 |
下列叙述正确的是( )
| A、某醋酸溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b |
| B、在滴有酚酞的氨水里,加入NH4Cl至溶液恰好无色,则此时溶液的pH<7 |
| C、常温下,1.0×10-3 mol?L-1盐酸的pH=3.0,1.0×10-8 mol?L-1盐酸的pH=8.0 |
| D、常温下,若1 mL pH=1的盐酸与100 mL NaOH溶液混合后,溶液的pH=7,则NaOH溶液的pH=11 |