题目内容
下列离子方程式书写不正确的是( )
| A、AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)=7:2时:2Al3++7OH-=Al(OH)3↓+AlO2-+2H2O |
| B、氨水吸收足量的SO2气体:NH3?H2O+SO2=NH4++HSO3- |
| C、高锰酸钾酸性溶液与草酸溶液反应:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O |
| D、向Fe(OH)3悬浊液中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.当n(OH-):n(Al3+)=7:2时,铝离子与氢氧根离子反应先生成氢氧化铝沉淀,然后部分氢氧化铝与氢氧根离子继续反应生成偏铝酸根;
B.一水合氨与足量二氧化硫反应生成亚硫酸氢铵;
C.高锰酸钾酸性溶液与草酸溶液发生氧化还原反应,生成锰离子、二氧化碳、水;
D.三价铁离子能够氧化碘离子.
B.一水合氨与足量二氧化硫反应生成亚硫酸氢铵;
C.高锰酸钾酸性溶液与草酸溶液发生氧化还原反应,生成锰离子、二氧化碳、水;
D.三价铁离子能够氧化碘离子.
解答:
解:A.AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+)=7:2时,离子方程式为:2Al3++7OH-=Al(OH)3↓+AlO2-+2H2O,故A正确;
B.氨水吸收足量的SO2气体,离子方程式:NH3?H2O+SO2=NH4++HSO3-,故B正确;
C.高锰酸钾酸性溶液与草酸溶液发生氧化还原反应,生成锰离子、二氧化碳、水,离子方程式:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O,故C正确;
D.向Fe(OH)3悬浊液中加入氢碘酸,离子方程式:2Fe(OH)3+2I-+6H+=2Fe2++6H2O+I2,故D错误;
故选:D.
B.氨水吸收足量的SO2气体,离子方程式:NH3?H2O+SO2=NH4++HSO3-,故B正确;
C.高锰酸钾酸性溶液与草酸溶液发生氧化还原反应,生成锰离子、二氧化碳、水,离子方程式:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O,故C正确;
D.向Fe(OH)3悬浊液中加入氢碘酸,离子方程式:2Fe(OH)3+2I-+6H+=2Fe2++6H2O+I2,故D错误;
故选:D.
点评:本题考查了离子方程式的书写,侧重考查氧化还原反应离子方程式书写、反应物用量不同发生反应不同的离子反应方程式书写,明确反应实质是解题关键,题目难度中等.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
下列各式中正确表示电解质电离的是( )
| A、H3PO4?T3H++PO43- |
| B、HCO3-+H2O?H3O++CO32- |
| C、CH3COONH4?CH3COO-+NH4+ |
| D、NaHS═Na++H++S2- |
设NA为阿伏加德罗常数,下列叙述正确的是( )
| A、2.4gMg与足量的盐酸反应失去的电子数为0.2NA |
| B、11.2L氯气所含的分子数为0.5NA |
| C、32g氧气中所含的氧原子数为NA |
| D、18g水中所含的电子数为8NA |
结合你所学的有机化学基础知识,判断下列说法中正确的是( )
| A、用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3 |
| B、将碘酒滴在鸡蛋清中,可观察到鸡蛋清显蓝色 |
| C、乙酸的酯化反应和苯的硝化反应属于同种反应类型 |
| D、乙烯能够发生加成反应,结构简式为CH2CH2 |
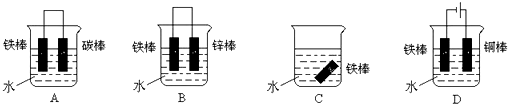
 三个课外实验小组用Na2SO3溶液、FeCl3溶液及其它试剂做了一系列实验:
三个课外实验小组用Na2SO3溶液、FeCl3溶液及其它试剂做了一系列实验: