题目内容
7.下列各组元素性质的递变情况正确的是( )| A. | Na、Mg、Al原子最外层电子数依次增多 | |
| B. | P、S、Cl元素最高正价依次降低 | |
| C. | N、O、F原子半径依次增大 | |
| D. | Na、K、Rb的金属性依次减弱 |
分析 A.根据原子核外电子排布分析;
B.根据元素的最高正价等于核外最外层电子数分析;
C.同周期,从左向右原子半径逐渐减小;
D.同主族元素从上到下元素的金属性依次增强.
解答 解:A.Na、Mg、Al原子最外层电子数分别为1、2、3,则原子最外层电子数依次增多,故A正确;
B.P、S、Cl原子最外层电子数分别为5、6、7,则P、S、Cl元素最高正价依次升高,故B错误;
C.同周期,原子半径从左向右逐渐减小,则N、O、F原子半径依次减小,故C错误;
D.同主族元素从上到下元素的金属性依次增强,则Na、K、Rb元素的金属性依次增强,故D错误.
故选A.
点评 本题考查元素周期律,明确同主族、同周期元素的性质变化规律是解答本题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.“绿色化学”对化学反应提出了“原子经济性”(原子节约)的新概念及要求,理想原子经济性反应是原料分子中的原子全部转化成所需要的产物,不产生副产物,实现零排放.下列反应类型一定符合这一要求的是( )
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤加聚反应 ⑥酯化反应.
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤加聚反应 ⑥酯化反应.
| A. | ①④ | B. | ②③ | C. | ⑤⑥ | D. | ②⑤ |
18.下列图象所表示的化学知识中,不正确的是( )
| A. | 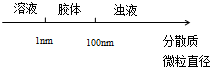 分散系的分类 | B. | 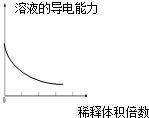 稀释浓氢氧化钠溶液的过程 | ||
| C. | 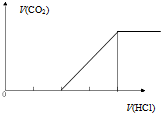 向碳酸钠溶液中逐滴滴加盐酸 | D. |  向偏铝酸钠溶液中逐滴滴加盐酸 |
15.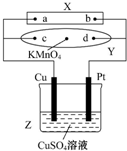 图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散.下列判断正确的是( )
图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散.下列判断正确的是( )
 图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散.下列判断正确的是( )
图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色斑向d端扩散.下列判断正确的是( )| A. | 滤纸上c点附近会变红色 | B. | Cu电极质量减小,Pt电极质量增大 | ||
| C. | Z中溶液的pH先减小,后增大 | D. | 溶液中的SO42-向Cu电极定向移动 |
2.下列叙述正确的是( )
①非金属元素构成的物质的化学键都是共价键
②两种不同非金属元素原子间形成的化学键都是极性键
③金属元素构成的化合物里一定含有离子键
④难失去电子的原子,易形成阴离子
⑤单质分子中不存在化学键,化合物的分子才存在化学键
⑥离子化合物中一定含有离子键.
①非金属元素构成的物质的化学键都是共价键
②两种不同非金属元素原子间形成的化学键都是极性键
③金属元素构成的化合物里一定含有离子键
④难失去电子的原子,易形成阴离子
⑤单质分子中不存在化学键,化合物的分子才存在化学键
⑥离子化合物中一定含有离子键.
| A. | 只有②⑥ | B. | 只有①⑤⑥ | C. | 只有③⑥ | D. | 只有①④⑥ |
12.下列关于能源的说法错误的是( )
| A. | 煤的干馏包括化学变化和物理变化 | |
| B. | 沼气(主要成分是CH4)是可再生能源 | |
| C. | 人类利用的能源都是通过化学反应获得的 | |
| D. | 石油是由1-50个碳原子的烷烃和环烷烃组成的混合物 |
17.下列各表中的数字代表的是元素的原子序数,表中数字所表示的元素与它们在周期表中的相对位置相符的是
( )
( )
| A. |
| B. |
| C. |
| D. |
|
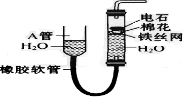 如图中的实验装置可用于制取乙炔. 请填空:
如图中的实验装置可用于制取乙炔. 请填空: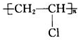 .
.