题目内容
16.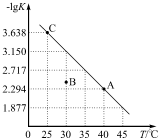 将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,在一定条件下发生下列反应:NH2COONH4(s)?2NH3(g)+CO2(g).该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示.下列说法不正确的是( )
将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,在一定条件下发生下列反应:NH2COONH4(s)?2NH3(g)+CO2(g).该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示.下列说法不正确的是( )| A. | 该反应的△H>0 | |
| B. | 30℃时,B点对应状态的v(正)<v(逆) | |
| C. | A点对应状态的平衡常数K(A)=10-2.294 | |
| D. | NH3的体积分数不变时,该反应一定达到平衡状态 |
分析 A、温度升高平衡常数的负对数(-lgK)减小,即温度越高K值越大;
B、30℃时,B点未平衡,最终要达平衡状态,平衡常数的负对数要变大,所以此时的(-lgQC)<(-lgK),所以QC>K;
C、A点对应平衡常数的负对数(-lgK)=2.294,所以A点对应状态的平衡常数K(A)=10-2.294;
D、体系中两种气体的物质的量之比始终不变.
解答 解:A、温度升高平衡常数的负对数(-lgK)减小,即温度越高K值越大,所以正反应是吸热反应,则△H>0,故A正确;
B、30℃时,B点未平衡,最终要达平衡状态,平衡常数的负对数要变大,所以此时的(-lgQC)<(-lgK),所以QC>K,所以B点对应状态的v(正)<v(逆),故B正确;
C、A点对应平衡常数的负对数(-lgK)=2.294,所以A点对应状态的平衡常数K(A)=10-2.294,故C正确;
D、体系中两种气体的物质的量之比始终不变,所以NH3的体积分数不变时,该反应不一定达到平衡状态,故D错误;
故选D.
点评 本题主要考查平衡状态的判断、平衡常数的计算、平衡移动的影响因素等,难度中等,解题时要注意氨基甲酸铵是固体.

练习册系列答案
相关题目
6.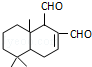 某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图(未表示出原子或原子团的空间排列).该拒食素与下列某试剂充分反应,所得有机物分子的官能团种类减少,则该试剂是( )
某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图(未表示出原子或原子团的空间排列).该拒食素与下列某试剂充分反应,所得有机物分子的官能团种类减少,则该试剂是( )
 某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图(未表示出原子或原子团的空间排列).该拒食素与下列某试剂充分反应,所得有机物分子的官能团种类减少,则该试剂是( )
某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图(未表示出原子或原子团的空间排列).该拒食素与下列某试剂充分反应,所得有机物分子的官能团种类减少,则该试剂是( )| A. | Br2的CCl4溶液 | B. | HBr | C. | Ag(NH3)2OH溶液 | D. | H2 |
7.下列有关物质应用的说法正确的是( )
| A. | 生石灰用作食品抗氧剂 | B. | 小苏打是面包发酵粉的主要成分 | ||
| C. | 铝罐可久盛食醋 | D. | 盐类都可作调味品 |
11.茉莉醛具有浓郁的茉莉花香,其结构简式如下所示: 关于茉莉醛的下列叙述不正确的是 (?)
关于茉莉醛的下列叙述不正确的是 (?)
 关于茉莉醛的下列叙述不正确的是 (?)
关于茉莉醛的下列叙述不正确的是 (?)| A. | 茉莉醛能使溴水褪色 | |
| B. | 在加热和催化剂作用下,能被氢气还原生成一种芳香醇 | |
| C. | 一定条件下,能被银氨溶液、新制氢氧化铜等多种氧化剂氧化 | |
| D. | 不能与氢溴酸发生加成反应 |
1.以硫酸铜溶液作电解液,对含有杂质Fe、Zn、Ag的粗铜进行电解精炼.下列叙述正确的是( )
| A. | 粗铜与直流电源负极相连 | |
| B. | 相同时间内阳极质量变化与阴极质量变化可能不同 | |
| C. | 硫酸铜溶液浓度始终保持不变 | |
| D. | 杂质Ag以Ag2SO4的形式沉入电解槽形成“阳极泥” |
8.乙醇(C2H5OH)和二甲醚(CH3OCH3)互为同分异构体且二甲醚不与钠反应.仅含碳、氢、氧三种元素的某化合物,其相对分子质量为88,且氧的质量分数为18.18%.已知该化合物不与钠反应,则该化合物的结构共有(不考虑立体异构)( )
| A. | 2种 | B. | 5种 | C. | 6种 | D. | 8种 |
5.在相同状况下,体积不相同的三个烧瓶中分别盛满了NH3、HCl和NO2,将它们倒扣在水槽中充分溶解后,塞住瓶口取出,烧瓶内三溶液物质的量浓度之比为( )
| A. | 1:1:1 | B. | 2:2:3 | C. | 3:3:2 | D. | 无法判断 |
 如图甲、乙是电化学实验装置.请回答下列问题:
如图甲、乙是电化学实验装置.请回答下列问题: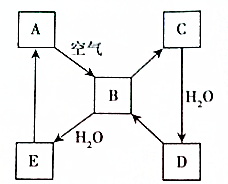 如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.
如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.