题目内容
有3中可溶性离子化合物A、B、C,共含六种离子,他们分别由阳离子NH4+、Na+、Cu2+和阴离子OH-、S2-、SO42-两两结合而成,取质量相等的A、B、C分别溶解于水,配成等体积的溶液,这3中溶液物质的量浓度大小的顺序是B<A<C并且B溶液呈蓝色.
根据题意回答下列问题:
(1)推断出A是 ,C是 .(填写化学式)
(2)室温时B溶液的pH 7.(填“>”“=”或“<”)
(3)向A溶液中加入适量的固体B,两者恰好完全反应,请写出反应的例子方程式 ;若反应前后溶液的体积相等,则原A溶液中的c(NH4+) 反应后所得溶液中c(NH4+).(填“>”“=”或“<”)
根据题意回答下列问题:
(1)推断出A是
(2)室温时B溶液的pH
(3)向A溶液中加入适量的固体B,两者恰好完全反应,请写出反应的例子方程式
考点:几组未知物的检验
专题:物质检验鉴别题
分析:由题意知A、B、C为可溶性离子化合物,可推断三种化合物的组成只能为(NH4)2S、NaOH、CuSO4,又知等质量的A、B、C配成等体积的溶液,物质的量浓度大小顺序为B<A<C并且B溶液呈蓝色,结合三种物质的式量,可确定 A、B、C分别为(NH4)2S、CuSO4、NaOH,以此解答该题.
解答:
解:(1)A、B、C为可溶性离子化合物,因Cu2+与OH-、S2-反应生成沉淀,NH4+与OH-反应生成弱电解质,可推断三种化合物的组成只能为(NH4)2S、NaOH、CuSO4,又知等质量的A、B、C配成等体积的溶液,物质的量浓度大小顺序为B<A<C,并且B溶液呈蓝色,结合三种物质的式量,可确定 A、B、C分别为(NH4)2S、CuSO4、NaOH,
故答案为:(NH4)2S;NaOH;
(2)硫酸铜溶液中,铜离子水解导致溶液显示酸性,pH<7,故答案为:<;
(3)向(NH4)2S溶液中加入固体CuSO4,二者反应生成硫化铜沉淀和硫酸铵,即S2-+Cu2+=CuS↓,在硫化铵中,硫离子对铵根离子的水解起促进作用,在反应后的硫酸铵溶液中,硫酸根离子不会影响铵根离子的水解,所以硫化铵中铵根离子浓度小于硫酸铵溶液中铵根离子浓度,
故答案为:S2-+Cu2+=CuS↓;<.
故答案为:(NH4)2S;NaOH;
(2)硫酸铜溶液中,铜离子水解导致溶液显示酸性,pH<7,故答案为:<;
(3)向(NH4)2S溶液中加入固体CuSO4,二者反应生成硫化铜沉淀和硫酸铵,即S2-+Cu2+=CuS↓,在硫化铵中,硫离子对铵根离子的水解起促进作用,在反应后的硫酸铵溶液中,硫酸根离子不会影响铵根离子的水解,所以硫化铵中铵根离子浓度小于硫酸铵溶液中铵根离子浓度,
故答案为:S2-+Cu2+=CuS↓;<.
点评:本题考查物质的检验和鉴别,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握离子的性质,为解答该题的关键,难度较大.

练习册系列答案
相关题目
关于键长、键能和键角,下列说法不正确的是( )
| A、键角是确定多分子立体结构(分子形状)的重要参数 |
| B、通过反应物和生成物分子中键能数据可以粗略预测反应热的大小 |
| C、键长越长,键能必越小,共价化合物必越稳定 |
| D、同种原子间形成的共价键键长长短总是遵循;叁键<双键<单键 |
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的内层电子总数是最外层电子数的5倍.下列说法中不正确的是( )
| A、W、M的某种单质可作为水处理中的消毒剂 |
| B、电解YW2的熔融物可制得Y和W的单质 |
| C、相同条件下,W的氢化物水溶液酸性比Z弱 |
| D、X、M两种元素形成的一种化合物与水反应可生成M的某种单质 |
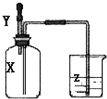 如图所示,集气瓶内充满某气体X,将滴管内的溶液Y挤入集气瓶后,烧杯中的溶液Z会进入集气瓶,然后又会有溶液被压回烧杯,则下列组合正确的是( )
如图所示,集气瓶内充满某气体X,将滴管内的溶液Y挤入集气瓶后,烧杯中的溶液Z会进入集气瓶,然后又会有溶液被压回烧杯,则下列组合正确的是( )| ① | X是甲烷,Y是高锰酸钾溶液,Z水 |
| ② | X是HCl,Y是浓硫酸,Z溴水 |
| ③ | X是氨气,Y是盐酸,Z浓氢氧化钠溶液 |
| ④ | X是SO2,Y是氢氧化钠溶液,Z浓硫酸 |
| A、①② | B、②④ | C、③④ | D、②③ |
下列有关用途的说法中,错误的是:( )
| A、液态钠可用作核反应堆的传热介质 |
| B、在过渡元素中找寻半导体材料 |
| C、考古时利用l4C测定一些文物的年代 |
| D、SiO2是制造水泥、人造宝石、单晶硅的原料 |
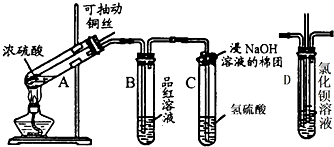
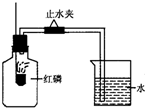 已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示:
已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示: