题目内容
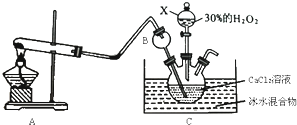
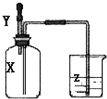 如图所示,集气瓶内充满某气体X,将滴管内的溶液Y挤入集气瓶后,烧杯中的溶液Z会进入集气瓶,然后又会有溶液被压回烧杯,则下列组合正确的是( )
如图所示,集气瓶内充满某气体X,将滴管内的溶液Y挤入集气瓶后,烧杯中的溶液Z会进入集气瓶,然后又会有溶液被压回烧杯,则下列组合正确的是( )| ① | X是甲烷,Y是高锰酸钾溶液,Z水 |
| ② | X是HCl,Y是浓硫酸,Z溴水 |
| ③ | X是氨气,Y是盐酸,Z浓氢氧化钠溶液 |
| ④ | X是SO2,Y是氢氧化钠溶液,Z浓硫酸 |
| A、①② | B、②④ | C、③④ | D、②③ |
考点:实验装置综合,氨的化学性质,氯、溴、碘及其化合物的综合应用,二氧化硫的化学性质
专题:元素及其化合物
分析:由图可知,烧杯中液体进入集气瓶的原因是存在压强差;当气体能与液体反应或溶于液体时,造成瓶内部压强变小,从而使烧杯中的液体进入集气瓶,然后又会有溶液被压回烧杯,说明又有气体生成,结合对应物质的性质解答该题.
解答:
解:①甲烷和高锰酸钾不反应,压强基本不变,故错误;
②HCl不溶于浓硫酸,压强基本不变,故错误;
③氨气与盐酸反应,压强减小,烧杯中的溶液氢氧化钠溶液会进入集气瓶,氢氧化钠和氯化铵反应生成氨气,压强又增大,则然后又会有溶液被压回烧杯,故正确;
④二氧化硫与氢氧化钠反应生成亚硫酸钠,压强减小,烧杯中的溶液浓硫酸会进入集气瓶,浓硫酸与亚硫酸钠反应生成二氧化硫气体,压强又增大,则然后又会有溶液被压回烧杯,故正确.
故选C.
②HCl不溶于浓硫酸,压强基本不变,故错误;
③氨气与盐酸反应,压强减小,烧杯中的溶液氢氧化钠溶液会进入集气瓶,氢氧化钠和氯化铵反应生成氨气,压强又增大,则然后又会有溶液被压回烧杯,故正确;
④二氧化硫与氢氧化钠反应生成亚硫酸钠,压强减小,烧杯中的溶液浓硫酸会进入集气瓶,浓硫酸与亚硫酸钠反应生成二氧化硫气体,压强又增大,则然后又会有溶液被压回烧杯,故正确.
故选C.
点评:本题综合考查元素化合物知识,侧重于学生的分析、实验能力的考查,注意气体发生反应的条件,充分理解压强变化带来的液体流动,难度不大.

练习册系列答案
 目标测试系列答案
目标测试系列答案
相关题目
下列化学用语表达正确的是( )
A、硝基苯的结构简式: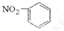 | ||
B、NH4Cl的电子式: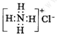 | ||
C、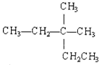 的名称为:3,3二甲基戍烷 的名称为:3,3二甲基戍烷 | ||
D、具有16个质子、16个种子和18个电子的微粒一定是
|