题目内容
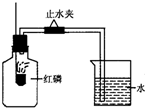 已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示:
已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示:(1)红磷在集气瓶中发生反应的化学方程式为
(2)待燃烧停止,白烟消失并冷却后,打开止水夹,观察到烧杯中的水进入集气瓶,瓶内水量约是集气瓶体积的
(3)若将红磷换成炭粉,该实验能否获得成功?
考点:实验装置综合
专题:实验题
分析:(1)红磷与氧气反应生成P2O5,红磷过量,可保证氧气完全反应;
(2)进入水的体积等于氧气的体积;氮气性质稳定,不溶于水,与红磷不反应;
(3)碳和氧气反应生成二氧化碳,为气体.
(2)进入水的体积等于氧气的体积;氮气性质稳定,不溶于水,与红磷不反应;
(3)碳和氧气反应生成二氧化碳,为气体.
解答:
解:(1)红磷与氧气反应生成P2O5,方程式为4P+5O2
2P2O5,红磷过量,可保证氧气完全反应,防止实验误差,
故答案为:4P+5O2
2P2O5;将瓶中氧气完全消耗掉;
(2)氧气和磷完全反应生成固体P2O5,进入水的体积等于氧气的体积,约为空气体积的
,该实验可推测氮气性质稳定,不溶于水,与红磷不反应,
故答案为:
;氮气难溶于水或氮气与红磷不反应;
(3)若将红磷换成炭粉,碳和氧气反应生成二氧化碳,为气体,瓶内压力不变,故答案为:否;碳粉消耗氧气生成二氧化碳,瓶内压力基本不变.
| ||
故答案为:4P+5O2
| ||
(2)氧气和磷完全反应生成固体P2O5,进入水的体积等于氧气的体积,约为空气体积的
| 1 |
| 5 |
故答案为:
| 1 |
| 5 |
(3)若将红磷换成炭粉,碳和氧气反应生成二氧化碳,为气体,瓶内压力不变,故答案为:否;碳粉消耗氧气生成二氧化碳,瓶内压力基本不变.
点评:本题考查空气中氧气含量的测定,侧重于学生的分析、实验能力的考查,注意把握测定的原理以及方法,把握物质的性质,难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
在与铝粉作用能放出氢气的溶液中,一定能大量共存的离子组是( )
| A、K+ Na+ SO42- Cl- |
| B、K+ Na+ S2- NO3- |
| C、Mg2+ NH4+ SO42- Cl- |
| D、K+ Na+ AlO2- ClO- |

 某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.
某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.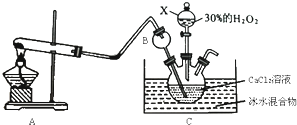


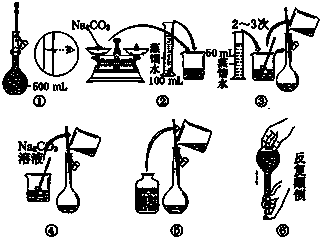 (1)若某药品质量约为32g
(1)若某药品质量约为32g