题目内容
下列过程中需要吸收热量的是( )
①N2→2N
②2Cl→Cl2
③SO3+H2O=H2SO4
④Zn+2HCl=ZnCl2+H2↑
⑤2KOH+H2SO4=2H2O+K2SO4
⑥2NH4Cl+Ba(OH)2=BaCl2+2NH3↑+2H2O
⑦食物腐败.
①N2→2N
②2Cl→Cl2
③SO3+H2O=H2SO4
④Zn+2HCl=ZnCl2+H2↑
⑤2KOH+H2SO4=2H2O+K2SO4
⑥2NH4Cl+Ba(OH)2=BaCl2+2NH3↑+2H2O
⑦食物腐败.
| A、①⑥ | B、①③⑥ |
| C、③④⑥⑦ | D、②③④⑤⑦ |
考点:反应热和焓变
专题:化学反应速率专题
分析:此题是一道关于物质发生化学反应时释放能量时吸热或放热的判断类型题,关于化学反应中是否是吸放热的判断,关键是掌握判断化学反应的基本方法,常见的放热反应有:所有的燃烧反应,金属与酸或水的反应、酸碱中和反应、多数的化合反应等,其△H<0.常见的吸热反应:Ba(OH)2?8H2O与NH4Cl晶体混合反应、水解反应、大多数的分解反应、以C、CO、H2作为还原剂的反应等,据此分析.
解答:
解:①拆开化学键需要吸收能量,故①正确;
②形成化学键能够释放能量,故②错误;
③化合反应大都放热,故③错误;
④活泼金属与酸反应是放热反应,故④错误;
⑤中和反应是放热反应,故⑤错误;
⑥氯化铵和氢氧化钡的反应是吸热反应,故⑥正确;
⑦食物腐败是缓慢氧化,是放热反应,故⑦错误;
故选A.
②形成化学键能够释放能量,故②错误;
③化合反应大都放热,故③错误;
④活泼金属与酸反应是放热反应,故④错误;
⑤中和反应是放热反应,故⑤错误;
⑥氯化铵和氢氧化钡的反应是吸热反应,故⑥正确;
⑦食物腐败是缓慢氧化,是放热反应,故⑦错误;
故选A.
点评:关于解答化学中吸热或放热的类型题时,应该熟练记住吸热或放热的判断规律,可以起到事半功倍的目的.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
对于易燃、易爆、有毒的化学物质,往往会在其包装上贴危险警告标签.下面所列物质中,贴错了标签的是
( )
| A | B | C | D | |
| 物质的 化学式 |
H2SO4(浓) | C2H5OH(酒精) | Hg(汞) | NaCl |
| 危险警 告标签 |
 |
 |
 |
 |
| A、A | B、B | C、C | D、D |
下列有关能量的叙述错误的是( )
| A、化学反应均伴随着能量的变化 |
| B、物质的化学能可以在一定条件下转化为热能、电能为人类利用 |
| C、吸热反应中由于反应物总能量小于生成物总能量,因而没有利用价值 |
| D、需要加热才能发生的反应不一定是吸热反应 |
下列表示方法正确的是( )
①H2S分子的比例模型: ②NH4Cl电子式:
②NH4Cl电子式:
③苯乙醛结构简式: ④丙烷分子的球棍模型:
④丙烷分子的球棍模型:
①H2S分子的比例模型:
 ②NH4Cl电子式:
②NH4Cl电子式:
③苯乙醛结构简式:
 ④丙烷分子的球棍模型:
④丙烷分子的球棍模型:
| A、①④ | B、①②④ |
| C、①②③④ | D、②③ |
下列说法错误的是( )
| A、需要加热方能发生的反应一定是吸热反应 |
| B、放热的反应在常温下不一定很容易发生 |
| C、反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小 |
| D、吸热反应在一定的条件下也能发生 |
下列离子反应方程式正确的是( )
A、铜粉与98.3%的硫酸加热下反应:Cu+4H++SO42-
| ||||
B、电解饱和食盐水:2Cl-+2H+
| ||||
| C、向氯化铝溶液中加入过量氨水:Al3++4NH3?H2O=[Al(OH)4]-+4NH4+ | ||||
| D、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:2Fe2++2H++H2O2=2Fe3++2H2O |
下列离子方程式中书写正确的是( )
| A、往氯化铝溶液中滴加过量氨水:Al3++4OH-═AlO2-+2H2O |
| B、用FeCl3溶液腐蚀印刷电路板:Fe3++Cu═Fe2++Cu2+ |
| C、向FeBr2溶液中通入过量氯气:2Br-+Cl2═Br2+2Cl- |
| D、NaOH溶液不能保存在玻璃塞的试剂瓶中:SiO2+2OH-═SiO32-+H2O |
下列有关化学用语使用正确的是( )
| A、CO2的电子式::O:C:O: |
| B、次氯酸的结构式:H-O-Cl |
C、中子数为18的氯原子结构示意图: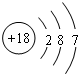 |
| D、二氧化硅的分子式为:SiO2 |