题目内容
下列表示方法正确的是( )
①H2S分子的比例模型: ②NH4Cl电子式:
②NH4Cl电子式:
③苯乙醛结构简式: ④丙烷分子的球棍模型:
④丙烷分子的球棍模型:
①H2S分子的比例模型:
 ②NH4Cl电子式:
②NH4Cl电子式:
③苯乙醛结构简式:
 ④丙烷分子的球棍模型:
④丙烷分子的球棍模型:
| A、①④ | B、①②④ |
| C、①②③④ | D、②③ |
考点:球棍模型与比例模型,电子式,结构简式
专题:化学用语专题
分析:①硫化氢分子的结构与水分子类型,为 V型结构;
②氯化铵的电子式中氯离子没有标出最外层电子;
③苯乙醛的结构简式中羟基的书写错误,应该为-CHO;
④用小球和短棍表示有机物分子组成的模型为球棍模型,根据丙烷的分子组成判断该球棍模型是否正确.
②氯化铵的电子式中氯离子没有标出最外层电子;
③苯乙醛的结构简式中羟基的书写错误,应该为-CHO;
④用小球和短棍表示有机物分子组成的模型为球棍模型,根据丙烷的分子组成判断该球棍模型是否正确.
解答:
解:①硫化氢分子中存在两个S-H键,为V型结构,所以H2S分子的比例模型为: ,故①正确;
,故①正确;
②氯化铵为离子化合物,阴离子需要标出最外层电子,NH4Cl正确的电子式为: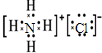 ,故②错误;
,故②错误;
③苯乙醛中醛基的表示方法错误,苯苯乙醛正确的结构简式为: ,故③错误;
,故③错误;
④丙烷结构简式为CH3CH2CH3,其丙烷分子的球棍模型为: ,故④正确;
,故④正确;
故选A.
 ,故①正确;
,故①正确;②氯化铵为离子化合物,阴离子需要标出最外层电子,NH4Cl正确的电子式为:
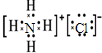 ,故②错误;
,故②错误;③苯乙醛中醛基的表示方法错误,苯苯乙醛正确的结构简式为:
 ,故③错误;
,故③错误;④丙烷结构简式为CH3CH2CH3,其丙烷分子的球棍模型为:
 ,故④正确;
,故④正确;故选A.
点评:本题考查了化学用语的表示方法判断,注意比例模型与球棍模型的表示方法,明确离子化合物与共价化合物的电子式的书写方法及区别,题目难度不大.

练习册系列答案
相关题目
下列物质中互为同分异构体的是( )
| A、甲烷和乙烷 |
| B、二氧化碳和干冰 |
| C、石墨和金刚石 |
| D、正丁烷和异丁烷 |
下列四种粒子的结构示意图中,属于稀有气体元素的原子是( )
A、 |
B、 |
C、 |
D、 |
下列有关化学用语表示正确的是( )
| A、乙炔的电子式H:C:::C:H |
B、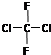 和 和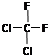 是同一物质 是同一物质 |
C、对甲基苯甲醇的结构简式: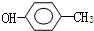 |
D、乙醇分子的比例模型: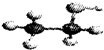 |
下列过程中需要吸收热量的是( )
①N2→2N
②2Cl→Cl2
③SO3+H2O=H2SO4
④Zn+2HCl=ZnCl2+H2↑
⑤2KOH+H2SO4=2H2O+K2SO4
⑥2NH4Cl+Ba(OH)2=BaCl2+2NH3↑+2H2O
⑦食物腐败.
①N2→2N
②2Cl→Cl2
③SO3+H2O=H2SO4
④Zn+2HCl=ZnCl2+H2↑
⑤2KOH+H2SO4=2H2O+K2SO4
⑥2NH4Cl+Ba(OH)2=BaCl2+2NH3↑+2H2O
⑦食物腐败.
| A、①⑥ | B、①③⑥ |
| C、③④⑥⑦ | D、②③④⑤⑦ |
以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的( )
| A、现有CO、CO2、O3三种气体,它们分别都含有1molO,则三种气体的物质的量之比为 3:2:1 |
| B、5.6g CO 和22.4L CO2中含有的碳原子数一定相等 |
| C、标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32 |
| D、n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为 35.5m/n |
在共价化合物中,元素化合价有正负的主要原因是( )
| A、电子有得失 |
| B、共用电子对有偏移 |
| C、电子既有得失又有电子对偏移 |
| D、有金属元素的存在 |
相同物质的量浓度的NaCN 和NaClO相比,NaCN溶液的pH较大,则同温同体积同浓度的HCN和HClO说法正确的是( )
| A、酸根离子浓度:c(CNˉ)<c(ClOˉ) |
| B、电离程度:HCN>HClO |
| C、pH:HClO>HCN |
| D、与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN |