题目内容
已知酒精(C2H5OH)能与K2Cr2O7,和H2SO4的混合溶液发生如下反应:
2K2Cr2O7+3C2H5OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O,且知Cr2O72-和Cr3+在溶液中分别显橙色和绿色,回答下列问题:
(1)该反应 (填“是”或“不是”)离子反应.
(2)写出电离方程式:Cr2(SO4)3: :K2Cr2O7
(3)该反应 (填“是”或“不是”)氧化还原反应,判断的依据是 .
(4)该反应能否用来检查司机是否酒后开车 (填“能”或“不能”),理由是 .
2K2Cr2O7+3C2H5OH+8H2SO4=2K2SO4+2Cr2(SO4)3+3CH3COOH+11H2O,且知Cr2O72-和Cr3+在溶液中分别显橙色和绿色,回答下列问题:
(1)该反应
(2)写出电离方程式:Cr2(SO4)3:
(3)该反应
(4)该反应能否用来检查司机是否酒后开车
考点:氧化还原反应,电离方程式的书写
专题:氧化还原反应专题
分析:(1)该反应中有离子参加反应,也有离子生成;
(2)均为强电解质,完全电离,遵循电荷守恒和原子守恒;
(3)反应中Cr元素的化合价降低,C元素的化合价升高;
(4)Cr2O72-和Cr3+在溶液中分别显橙色和绿色,可利用颜色的变化检验乙醇.
(2)均为强电解质,完全电离,遵循电荷守恒和原子守恒;
(3)反应中Cr元素的化合价降低,C元素的化合价升高;
(4)Cr2O72-和Cr3+在溶液中分别显橙色和绿色,可利用颜色的变化检验乙醇.
解答:
解:(1)该反应中有离子参加反应,也有离子生成,所以该反应是离子反应,故答案为:是;
(2)均为强电解质,完全电离,遵循电荷守恒和原子守恒,电离方程式分别为Cr2(SO4)3=2Cr3++3SO42-、K2Cr2O7=2K++Cr2O72-,
故答案为:Cr2(SO4)3=2Cr3++3SO42-;K2Cr2O7=2K++Cr2O72-;
(3)反应中Cr元素的化合价降低,C元素的化合价升高,则该反应是氧化还原反应,故答案为:是;元素的化合价有升降(或发生了电子转移);
(4)Cr2O72-和Cr3+在溶液中分别显橙色和绿色,可利用颜色的变化检验乙醇,即橙色的Cr2O72-在酒精作用下转化为绿色的Cr3+,则能检查司机是否酒后开车,
故答案为:能;橙色的Cr2O72-在酒精作用下转化为绿色的Cr3+.
(2)均为强电解质,完全电离,遵循电荷守恒和原子守恒,电离方程式分别为Cr2(SO4)3=2Cr3++3SO42-、K2Cr2O7=2K++Cr2O72-,
故答案为:Cr2(SO4)3=2Cr3++3SO42-;K2Cr2O7=2K++Cr2O72-;
(3)反应中Cr元素的化合价降低,C元素的化合价升高,则该反应是氧化还原反应,故答案为:是;元素的化合价有升降(或发生了电子转移);
(4)Cr2O72-和Cr3+在溶液中分别显橙色和绿色,可利用颜色的变化检验乙醇,即橙色的Cr2O72-在酒精作用下转化为绿色的Cr3+,则能检查司机是否酒后开车,
故答案为:能;橙色的Cr2O72-在酒精作用下转化为绿色的Cr3+.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,注意反应类型的判断及化学与生活的关系,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列反应中属于氧化还原反应的是( )
A、NH4HCO3
| ||||
| B、Na2O+H2O═2NaOH | ||||
| C、Na2CO3+H2SO4═Na2SO4+CO2↑+H2O | ||||
D、2H2O
|
下列各组物质可以用分液漏斗分离的是( )
| A、酒精和水 | B、苯和水 |
| C、乙醇和乙酸乙酯 | D、乙酸和水 |
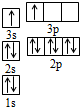 有A、B、C、D四种元素.已知A原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大.B 的基态原子占据两种形状的原子轨道,且两种形状轨道中的电子总数均相同,B位于元素周期表的s区.C元素原子的外围电子层排布式为nsn-1npn-1. D原子M能层为全充满状态,且核外的未成对电子只有一个.请回答下列问题:
有A、B、C、D四种元素.已知A原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大.B 的基态原子占据两种形状的原子轨道,且两种形状轨道中的电子总数均相同,B位于元素周期表的s区.C元素原子的外围电子层排布式为nsn-1npn-1. D原子M能层为全充满状态,且核外的未成对电子只有一个.请回答下列问题: