题目内容
下列离子反应方程式正确的是( )
A、铜粉与98.3%的硫酸加热下反应:Cu+4H++SO42-
| ||||
B、电解饱和食盐水:2Cl-+2H+
| ||||
| C、向氯化铝溶液中加入过量氨水:Al3++4NH3?H2O=[Al(OH)4]-+4NH4+ | ||||
| D、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:2Fe2++2H++H2O2=2Fe3++2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A、从浓硫酸不能拆的角度来分析.
B、弱电解质不能拆.
C、从产物是否正确来分析.
D、双氧水将亚铁离子给氧化为三价铁离子.
B、弱电解质不能拆.
C、从产物是否正确来分析.
D、双氧水将亚铁离子给氧化为三价铁离子.
解答:
解:A、铜粉与98.3%的硫酸加热下反应化学方程式:Cu+2H2SO4
CuSO4+SO2↑+2H2O,而98.3%的硫酸为浓硫酸,不能拆,故离子方程式应为:Cu+2H2SO4
Cu2++SO42++SO2↑+2H2O,故A错误;
B、电解饱和食盐水化学方程式:2NaCl+2H2O
H2↑+C12↑+2NaOH,水为弱电解质,不能拆,故离子方程式为:2Cl-+2H2O
H2↑+C12↑+2OH-,故B错误;
C、向氯化铝溶液中加入过量氨水:AlCl3+3NH3?H2O=Al(OH)3↓+3NH4Cl,故离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故C错误;
D、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液发生反应:2FeSO4+H2SO4+H2O2=Fe2(SO4)3+2H2O,故离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O,故D正确.
故选D.
| ||
| ||
B、电解饱和食盐水化学方程式:2NaCl+2H2O
| ||
| ||
C、向氯化铝溶液中加入过量氨水:AlCl3+3NH3?H2O=Al(OH)3↓+3NH4Cl,故离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故C错误;
D、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液发生反应:2FeSO4+H2SO4+H2O2=Fe2(SO4)3+2H2O,故离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O,故D正确.
故选D.
点评:本题考查了离子方程式的书写,从物质的拆分、产物是否正确、电荷守恒等角度来分析.

练习册系列答案
相关题目
下列四种粒子的结构示意图中,属于稀有气体元素的原子是( )
A、 |
B、 |
C、 |
D、 |
下列过程中需要吸收热量的是( )
①N2→2N
②2Cl→Cl2
③SO3+H2O=H2SO4
④Zn+2HCl=ZnCl2+H2↑
⑤2KOH+H2SO4=2H2O+K2SO4
⑥2NH4Cl+Ba(OH)2=BaCl2+2NH3↑+2H2O
⑦食物腐败.
①N2→2N
②2Cl→Cl2
③SO3+H2O=H2SO4
④Zn+2HCl=ZnCl2+H2↑
⑤2KOH+H2SO4=2H2O+K2SO4
⑥2NH4Cl+Ba(OH)2=BaCl2+2NH3↑+2H2O
⑦食物腐败.
| A、①⑥ | B、①③⑥ |
| C、③④⑥⑦ | D、②③④⑤⑦ |
以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的( )
| A、现有CO、CO2、O3三种气体,它们分别都含有1molO,则三种气体的物质的量之比为 3:2:1 |
| B、5.6g CO 和22.4L CO2中含有的碳原子数一定相等 |
| C、标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32 |
| D、n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为 35.5m/n |
某无色溶液中存在大量的H+、NH4+、SO42-,该溶液中还可能存在的离子是( )
| A、K+ |
| B、Ba2+ |
| C、OH- |
| D、HCO3- |
在共价化合物中,元素化合价有正负的主要原因是( )
| A、电子有得失 |
| B、共用电子对有偏移 |
| C、电子既有得失又有电子对偏移 |
| D、有金属元素的存在 |
已知离子 bX3+ 的离子结构示意图为: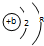 ,下列认识正确的是( )
,下列认识正确的是( )
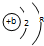 ,下列认识正确的是( )
,下列认识正确的是( )| A、b=10 |
| B、X单质能溶于氢氧化钠溶液 |
| C、X为稀有气体 |
| D、X单质既具有还原性,又具有氧化性 |
已知有如下反应:
①2BrO
+Cl2═Br2+2ClO
;
②ClO
+5Cl-+6H+═3Cl2+3H2O;
③2FeCl3+2KI═2FeCl2+2KCl+I2;
④2FeCl2+Cl2═2FeCl3.
下列叙述正确的是( )
①2BrO
- 3 |
- 3 |
②ClO
- 3 |
③2FeCl3+2KI═2FeCl2+2KCl+I2;
④2FeCl2+Cl2═2FeCl3.
下列叙述正确的是( )
A、氧化能力:ClO
| ||||
| B、还原能力:Fe2+>I->Cl- | ||||
C、反应ClO
| ||||
D、氧化能力:BrO
|
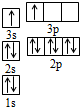 有A、B、C、D四种元素.已知A原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大.B 的基态原子占据两种形状的原子轨道,且两种形状轨道中的电子总数均相同,B位于元素周期表的s区.C元素原子的外围电子层排布式为nsn-1npn-1. D原子M能层为全充满状态,且核外的未成对电子只有一个.请回答下列问题:
有A、B、C、D四种元素.已知A原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大.B 的基态原子占据两种形状的原子轨道,且两种形状轨道中的电子总数均相同,B位于元素周期表的s区.C元素原子的外围电子层排布式为nsn-1npn-1. D原子M能层为全充满状态,且核外的未成对电子只有一个.请回答下列问题: