题目内容
化学用语是表示物质组成、结构和变化规律的一种具有国际性、科学性和规范性的书面语言.下列化学用语中,书写错误的是( )
A、硫离子的结构示意图: |
B、NH4Cl的电子式: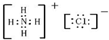 |
C、CO2的电子式: |
| D、次氯酸的结构式:H-O-Cl |
考点:电子式、化学式或化学符号及名称的综合,原子结构示意图
专题:
分析:A.硫离子的核电荷数为16,核外电子总数为18;
B.氯化铵属于离子化合物,电子式中需要标出阴阳离子所带电荷;
C.二氧化碳分子中存在两个碳氧双键;
D.次氯酸分子中存在1个氧氢键和1个氧氯键.
B.氯化铵属于离子化合物,电子式中需要标出阴阳离子所带电荷;
C.二氧化碳分子中存在两个碳氧双键;
D.次氯酸分子中存在1个氧氢键和1个氧氯键.
解答:
解:A.硫离子的核外电子总数为18,最外层为8个电子,硫离子的结构示意图为: ,故A正确;
,故A正确;
B.铵根离子为复杂阳离子,所以铵根离子和氯离子都需要标出最外层电子,则NH4Cl的电子式为: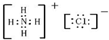 ,故B正确;
,故B正确;
C.二氧化碳为共价化合物,分子中存在两个碳氧双键,不存在碳氧单键,二氧化碳正确的电子式为: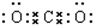 ,故C错误;
,故C错误;
D.次氯酸的中心原子为O原子,其分子中存在1个氧氢键和1个氧氯键,次氯酸的结构式为:H-O-Cl,故D正确;
故选C.
 ,故A正确;
,故A正确;B.铵根离子为复杂阳离子,所以铵根离子和氯离子都需要标出最外层电子,则NH4Cl的电子式为:
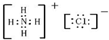 ,故B正确;
,故B正确;C.二氧化碳为共价化合物,分子中存在两个碳氧双键,不存在碳氧单键,二氧化碳正确的电子式为:
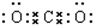 ,故C错误;
,故C错误;D.次氯酸的中心原子为O原子,其分子中存在1个氧氢键和1个氧氯键,次氯酸的结构式为:H-O-Cl,故D正确;
故选C.
点评:本题考查了常见化学用语的判断,题目难度中等,注意掌握电子式、原子结构示意图与离子结构示意图、结构式等化学用语的概念及书写原则,D为易错点,注意明确次氯酸的结构.

练习册系列答案
相关题目
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
| A、电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ |
| B、氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- |
| C、粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-═Cu2+ |
| D、钢铁发生电化学腐蚀的正极反应式:Fe-2e-═Fe3+ |
A,B两元为某周期ⅡA族和ⅢA族元素,若A的原子序数为x,则B的原子序数可能是( )
①x+1 ②x+81 ③x+11 ④x+18 ⑤x+25.
①x+1 ②x+81 ③x+11 ④x+18 ⑤x+25.
| A、①③ | B、②④ |
| C、①③⑤ | D、②③④⑤ |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、常温常压下,15g甲基(-CH3)中所含的中子数为6NA |
| B、一定条件下Fe粉与足量的浓硫酸反应,转移电子数为3NA |
| C、在1 L的碳酸钠溶液中,若c(CO32-)=1 mol?L-1,则溶液中Na+的个数为2NA |
| D、含4NA个离子的固体Na2O2溶于水配成1 L溶液,所得溶液中Na+的物质的量浓度为2 mol?L-1 |
下列各组在溶液中的反应,不管反应物的量是多少,都能用同一离子方程式表示的是( )
| A、NaOH与CO2 |
| B、Ba(OH)2与H2SO4 |
| C、HC1与Na2CO3 |
| D、NaHCO3与Ca(OH)2 |
下列溶液中有关物质的量浓度关系正确的是( )
| A、pH=2的HA溶液与pH=12的MOH溶液任意比混合:[H+]+[M+]=[OH-]+2[A-] |
| B、pH相等的CH3COONa、NaOH和Na2CO3三种溶液:[NaOH]<[CH3COONa]<[Na2CO3] |
| C、物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:[CH3COO-]+2[OH-]=2[H+]+[CH3COOH] |
| D、0.1 mol?L-1的NaHA溶液,其pH=4,则[HA-]>[H+]>[H2A]>[A2-] |
 . CH3CH=CHCH3是石油裂解的产物之一,它的键线式结构可表示为
. CH3CH=CHCH3是石油裂解的产物之一,它的键线式结构可表示为 .
. +Br2→
+Br2→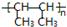 是一种加聚产物,则其单体的结构简式为
是一种加聚产物,则其单体的结构简式为 课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图所示连接,C、D、E、F、X、Y 都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.试回答下列问题:
课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图所示连接,C、D、E、F、X、Y 都是惰性电极.将电源接通后,向乙中滴入酚酞试液,在F极附近显红色.试回答下列问题: