题目内容
11.某无色废水中可能含有Fe3+、Al3+、Mg2+、Na+、NO3-、Cl-、SO42-离子中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关现象如图:
回答下列问题:
(1)焰色反应的操作步骤简记为洗、烧、蘸、烧、洗,洗铂丝的试剂是盐酸(写名称),若采用焰色反应检测K+时,观察火焰焰色时必须要透过蓝色钴玻璃观察.
(2)实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除烧杯、玻璃棒、托盘天平、量筒、药匙、胶头滴管,还缺少的仪器为100mL容量瓶.
(3)实验③中沉淀量由A→B过程中所发生反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(4)经分析,该溶液中肯定存在的阳离子有Al3+、Mg2+.
(5)现补充第④组实验:另取100mL废水,加入硝酸酸化,再滴入AgNO3溶液,未见白色沉淀生成,则该废水中一定存在的阴离子除SO42-还有NO3-.
分析 无色废水确定无Fe3+,根据实验①确定无Na+,根据实验②确定有SO42-,根据实验③确定有Al3+和Mg2+,故溶液中存在的离子为:Al3+、Mg2+、SO42-,根据硫酸钡沉淀求出n(SO42-),根据图象求出n(Al3+)和n(Mg2+),再根据电荷守恒确定有没有NO3-,以此解答该题.
解答 解:无色废水确定无Fe3+,根据实验①确定无Na+,根据实验②确定有SO42-,根据实验③确定有Al3+和Mg2+,故溶液中存在的离子为:Al3+、Mg2+、SO42-,根据硫酸钡沉淀求出n(SO42-),根据图象求出n(Al3+)和n(Mg2+),再根据电荷守恒确定有没有NO3-,
(1)焰色反应的操作步骤简记为洗、烧、蘸、烧、洗,洗铂丝的试剂是盐酸,为避免黄色光的干扰,滤去黄光,在观察K+的焰色时,必须要透过蓝色钴玻璃观察,
故答案为:盐酸;蓝色钴玻璃;
(2)配制1.0mol/L的NaOH溶液100mL,根据实验步骤所需仪器:玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管、100mL容量瓶、烧杯,
故答案为:100mL容量瓶;
(3)实验③中A→B过程是Al(OH)3与OH-发生反应,其方程式为:Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)由以上分析可知溶液中存在的离子为:Al3+、Mg2+、SO42-,所以肯定存在的阳离子是Al3+、Mg2+,
故答案为:Al3+、Mg2+;
(5)液中存在的离子为:Al3+、SO42-、Mg2+,已知硫酸钡沉淀为2.33g,则n(SO42-)=$\frac{2.33g}{233g/mol}$=0.01mol,
根据图象可知与Al(OH)3的OH-为:n(OH-)=0.005mol,
Al(OH)3 +OH-=AlO2-+2H2O Mg2++2OH-=Fe(OH)2↓
n(Al3+) 0.005mol n(Mg2+) 0.035-3n(Al3+)
所以n(Al3+)=0.005mol,n(Mg2+)=0.01mol 所以溶液中Mg2+和Al3+所带正电荷与SO42-所带负电荷不相等,加入硝酸酸化,再滴入AgNO3溶液,未见白色沉淀生成,则一定不存在Cl-,因此存在NO3-,
故答案为:NO3-.
点评 本题考查无机物的推断,为高频考点,侧重于学生的分析、计算能力的考查,关键是图象分析离子特征和离子共存的判断,题目难度中等.

| A. | 辛烯和1-丁烯 | B. | 苯和乙炔 | ||
| C. | 1-氯丙烷和2-氯丙烷 | D. | 甲基环己烷和乙烯 |
(1)在一定条件下,在20L密闭容器中按物质的量比为1:3充入CO2和H2,温度在450K,n(H2)随时间变化如下表所示:
| t/min | 0 | 1 | 3 | 5 |
| N(H2)/mol | 8 | 6 | 5 | 5 |
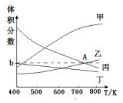
(2)在5MPa下测得平衡体系中各物质的体积分数随温度的变化曲线如图所示:曲线乙表示的是CO2(填物质的化学式)的体积分数,图象中A点对应的体积分数b=18.8%(结果保留三位有效数字).
(3)下列措施中能使化学平衡向正反应方向移动的是BD
A.升高温度 B.将CH3CH2OH(g)及时液化抽出
C.选择高效催化剂 D.再充入l molCO2和3molH2
(4)25℃,1.01×105Pa时,9.2g液态乙醇完全燃烧,当恢复到原状态时,放出273.4kJ的热量,写出表示乙醇燃烧的热化学方程式:CH3CH2OH(l)+3O2(g)═CO2(g)+2H2O(l)△H=-1367kJ•mol-1.
(5)以石墨为电极,氢氧化钠、乙醇、水、氧气为原料,可以制成乙醇的燃料电池,写出发生还原反应的电极反应式:O2+2H2O+4e-═4OH?.
| A. | 标准状况下,VL水含有的氧原子个数约为V/22.4 NA | |
| B. | 常温常压下,1 mol 碳烯( CH2)所含的电子总数为8NA | |
| C. | 标准状况下,含NA个氩原子的氩气体积约为22.4L | |
| D. | 1mol OH-参与电解,提供的电子数目为NA个 |
| 时间 水样 | 0 | 5 | 10 | 15 | 20 | 25 |
| Ⅰ(pH=2) | 0.4 | 0.28 | 0.19 | 0.13 | 0.10 | 0.09 |
| Ⅱ(pH=4) | 0.4 | 0.31 | 0.24 | 0.20 | 0.18 | 0.16 |
| Ⅲ(pH=4) | 0.20 | 0.15 | 0.12 | 0.09 | 0.07 | 0.05 |
| Ⅳ(pH=4,含Ca2+) | 0.20 | 0.09 | 0.05 | 0.03 | 0.01 | 0 |
| A. | 在0~20 min内,Ⅰ中M的分解速率为0.015 mol•L-1•min-1 | |
| B. | 水样酸性越强,M的分解速率越快 | |
| C. | 在0~20 min内,Ⅲ中M的分解百分率比Ⅱ大 | |
| D. | 由于Ca2+存在,Ⅳ中M的分解速率比Ⅰ快 |
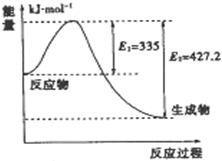 到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.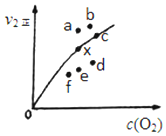 利用化学反应原理研究氮和硫的化合物有重要意义.
利用化学反应原理研究氮和硫的化合物有重要意义.
 .
.