题目内容
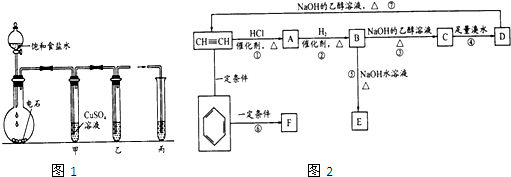
如图所示是用于气体制备、干燥(或除杂质)、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去,各装置可重复使用也可不用).请根据下列要求回答问题.

(1)若用A-C-D-B组合进行氢气还原氧化铜实验.分液漏斗中的试剂是盐酸,C中试剂是水,其作用是 ;A中反应开始一段时间后,再加热B.加热B之前的实验操作是 .
(2)为验证氯气不能使干燥的红布条褪色,置红布条于B中,按A-C-B-D连接成实验装置体系.A锥形瓶中试剂选用高锰酸钾晶体,则分液漏斗中的液体是 (填名称);C中试剂是 (填名称).已知高锰酸钾反应生成+2价的锰离子,写出此法制备氯气的离子方程式 .
(3)为了进行氨的催化氧化实验,若锥形瓶中盛装足量的Na2O2粉末,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞,产生的气体通过红热的铂粉,各仪器装置按气流方向从左到右连接顺序是(填字母) ;装置B中发生反应的化学方程式为 .

(1)若用A-C-D-B组合进行氢气还原氧化铜实验.分液漏斗中的试剂是盐酸,C中试剂是水,其作用是
(2)为验证氯气不能使干燥的红布条褪色,置红布条于B中,按A-C-B-D连接成实验装置体系.A锥形瓶中试剂选用高锰酸钾晶体,则分液漏斗中的液体是
(3)为了进行氨的催化氧化实验,若锥形瓶中盛装足量的Na2O2粉末,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞,产生的气体通过红热的铂粉,各仪器装置按气流方向从左到右连接顺序是(填字母)
考点:常见气体制备原理及装置选择,性质实验方案的设计
专题:实验设计题
分析:(1)C中水的作用是洗气,即吸收氢气中混有HCl;加热B之前必须检验氢气的纯度,防止氢气不纯时发生爆炸;加热后黑色固体变为红色;
(2)高锰酸钾和浓盐酸制备氯气,因此分液漏斗中为浓盐酸,氯气和水能反应生成HClO,所以需要用浓硫酸干燥氯气,依据反应物和已知产物结合得失电子守恒、质量守恒写出离子方程式并配平;
(3)过氧化钠与水反应生成氧气,与氨气经干燥后在催化剂的作用下反应生成NO,剩余气体必须进行尾气处理;氨气和氧气在催化剂加热条件下反应生成NO和水.
(2)高锰酸钾和浓盐酸制备氯气,因此分液漏斗中为浓盐酸,氯气和水能反应生成HClO,所以需要用浓硫酸干燥氯气,依据反应物和已知产物结合得失电子守恒、质量守恒写出离子方程式并配平;
(3)过氧化钠与水反应生成氧气,与氨气经干燥后在催化剂的作用下反应生成NO,剩余气体必须进行尾气处理;氨气和氧气在催化剂加热条件下反应生成NO和水.
解答:
解:(1)C中水的作用是洗气,由于盐酸一挥发,所以水可以吸收氢气中混有HCl;加热B之前必须检验氢气的纯度,防止氢气不纯时发生爆炸,
故答案为:吸收氢气中的HCl;检验氢气纯度;
(2)高锰酸钾和浓盐酸制备氯气,因此分液漏斗中为浓盐酸,氯气和水能反应生成HClO,HClO能使有色布条褪色,因此需要用浓硫酸干燥氯气,过氧化钠与水反应的离子方程式为:2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O,
故答案为:浓盐酸;浓硫酸;2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O;
(3)过氧化钠与水反应生成氧气,与氨气经盛有碱石灰的干燥管干燥后在催化剂的作用下反应生成NO,剩余气体必须进行尾气处理,则连接顺序为A→D→B→C(C盛装氢氧化钠溶液);氨气和氧气在催化剂加热条件下反应生成NO和水,化学方程式为:4NH3+5O2
4NO+6H2O,
故答案为:A→D→B→C;4NH3+5O2
4NO+6H2O.
故答案为:吸收氢气中的HCl;检验氢气纯度;
(2)高锰酸钾和浓盐酸制备氯气,因此分液漏斗中为浓盐酸,氯气和水能反应生成HClO,HClO能使有色布条褪色,因此需要用浓硫酸干燥氯气,过氧化钠与水反应的离子方程式为:2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O,
故答案为:浓盐酸;浓硫酸;2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O;
(3)过氧化钠与水反应生成氧气,与氨气经盛有碱石灰的干燥管干燥后在催化剂的作用下反应生成NO,剩余气体必须进行尾气处理,则连接顺序为A→D→B→C(C盛装氢氧化钠溶液);氨气和氧气在催化剂加热条件下反应生成NO和水,化学方程式为:4NH3+5O2
| ||
| △ |
故答案为:A→D→B→C;4NH3+5O2
| ||
| △ |
点评:本题考查少量氨气的制备和氯气的制备,综合性较强,难度中等,并验证二者的化学性质,涉及气体制备、干燥(或除杂质)、性质验证、尾气处理,掌握常见气体的制备原理和除杂是解题关键,

练习册系列答案
相关题目
下列实验操作或方法中,不正确的是( )
A、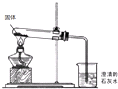 区别碳酸钠和碳酸氢钠 |
B、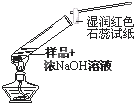 检验试液中NH4+的存在 |
C、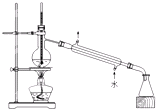 实验室蒸馏石油 |
D、 过滤操作 |
现在配制100mL 1mol/L NaOH溶液,下列操作正确的是( )
| A、在托盘天平的两个托盘上各放一张大小一样的纸,然后将氢氧化钠固体放在纸片上进行称量 |
| B、用蒸馏水洗涤烧杯、玻璃棒2-3次,每次洗涤后的溶液都注入容量瓶中 |
| C、把称量的NaOH固体放入盛有适量蒸馏水的烧杯中,溶解后立即把溶液移入100mL容量瓶中 |
| D、沿着玻璃棒往容量瓶中加入蒸馏水,直到溶液凹液面恰好与刻度相切 |