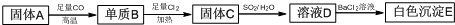题目内容
9.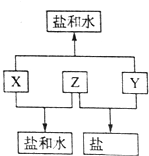 已知:A、B、C、D四种短周期元素,A与D原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,已知Z是常见的两性氢氧化物,试推断回答下列问题.
已知:A、B、C、D四种短周期元素,A与D原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,已知Z是常见的两性氢氧化物,试推断回答下列问题.(1)D元素原子的结构示意图为
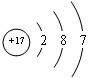 ;
;(2)A、B、C三种元素的原子半径由小到大的顺序为N<Al<Na(用元素符号表示);
(3)Y与C元素的最高价氧化物可以发生反应,该反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O;
(4)实验室中,应将X的浓溶液保存在棕色试剂瓶中,其原因是4HNO3$\frac{\underline{\;光照\;}}{\;}$4NO2↑+2H2O+O2↑(用化学方程式表示).
分析 A、B、C、D四种短周期元素,D元素组成的单质在通常状况下呈黄绿色,所以D是Cl元素;A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,由框图转化关系可知应是氢氧化铝、强酸、强碱之间的反应,B、C、D三种元素位于同一周期,Z是常见的两性氢氧化物,则C为Al,Z为Al(OH)3,B为Na,Y为NaOH,而A与D(氯)原子序数之和等于B与C的原子序数之和,则A为N,X为HNO3.
解答 解:A、B、C、D四种短周期元素,D元素组成的单质在通常状况下呈黄绿色,所以D是Cl元素;A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,由框图转化关系可知应是氢氧化铝、强酸、强碱之间的反应,B、C、D三种元素位于同一周期,Z是常见的两性氢氧化物,则C为Al,Z为Al(OH)3,B为Na,Y为NaOH,而A与D(氯)原子序数之和等于B与C的原子序数之和,则A为N,X为HNO3.
(1)Cl元素原子核外电子数为17,有3个电子层,各层电子数为2、8、7,原子结构示意图为 ,故答案为:
,故答案为: ;
;
(2)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径N<Al<Na,故答案为:N<Al<Na;
(3)氢氧化钠与氢氧化铝反应生成偏铝酸钠与水,反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(4)X为HNO3,不稳定,见光易分解,应保存在棕色瓶中,反应的方程式为4HNO3$\frac{\underline{\;光照\;}}{\;}$4NO2↑+2H2O+O2↑,
故答案为:4HNO3$\frac{\underline{\;光照\;}}{\;}$4NO2↑+2H2O+O2↑.
点评 本题考查无机物的推断,D物质的颜色及Z是两性氢氧化物是推断突破口,熟练掌握元素化合物性质,题目难度中等.

| A. | NaHCO3 的电离:NaHCO3═Na++H++CO32- | |
| B. | HS-的电离:HS-+H2O?H3O ++S2- | |
| C. | NaClO的电离:NaClO?Na++ClO- | |
| D. | NH4Cl水解方程式 NH4++H2O═NH3•H2O+H+ |
| A. | 用pH试纸测定新制氯水的pH=2 | |
| B. | 用玻璃棒在过滤器上搅拌以加速硫酸铜晶体的洗涤 | |
| C. | 向某溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀生成,则该溶液中不一定含有SO${\;}_{4}^{2-}$ | |
| D. | 向可溶性淀粉溶液中滴加碘酒,溶液呈蓝色,用CCl4作萃取剂振荡、静置后,下层呈紫红色 |
| A. | 碘化钾溶液中加入浓溴水2I-+Br2═2Br-+I2 | |
| B. | 小苏打与盐酸反应CO32-+2H+═CO2↑+H2O | |
| C. | 氯化铁溶液中加入铁粉:2Fe3++Fe═3Fe2+ | |
| D. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
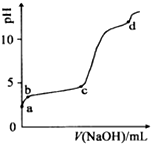
| A. | a点溶液呈酸性的原因是Al3+水解,离子方程为:Al3++3OH-?Al(OH)3 | |
| B. | c点铝元素主要以Al(OH)3的形式存在 | |
| C. | a-b段,溶液pH增大,Al3+浓度不变 | |
| D. | d点Al(OH)3沉淀开始溶解 |
(1)铜元素在元素周期表中的位置为第四周期ⅠB族,Cu+的核外电子排布式为1s22s22p63s23p63d10或[Ar]3d10,基态铜原子核外电子共有29种运动状态.
(2)Cu2S在一定条件下可被氧化为CuSO4.
①在SO42-中S原子的杂化轨道类型为sp3;SiO44-、PO43-与 SO42-互为等电子体;其中Si、P、S第一电离能由大到小顺序为P>S>Si;
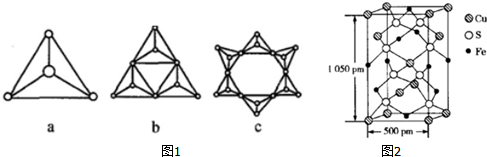
②硅酸盐与二氧化硅一样,都是以硅氧四面体作为基本结构单元,硅氧四面体可以用图1a 表示,图1中b、c 是硅氧四面体结合成环状结构的两个例子,若在环状结构中硅的原子数为n,写出环状结构中硅酸根离子的通式SinO3n2n-.
(3)甲醇(CH3OH)中的羟基被硫羟基取代生成甲硫醇(CH3SH),二者部分物理性质如表:
| 物质 | 熔点/℃ | 沸点/℃ | 水溶液 |
| 甲醇 | -97 | 64.7 | 互溶 |
| 甲硫醇 | -123 | 6.8 | 不溶 |
(4)某化合物由S、Fe、Cu 三种元素组成,其晶胞结构如图2所示(1pm=10-10cm),该晶胞上下底面为正方形,侧面与底面垂直,则该晶体的密度ρ=4.66g/cm3(保留三位有效数字).
| A. | H2O | B. | CH3OH | C. | CS2 | D. | CH3COOH |
| A. | 18 g H2O所含的分子数为NA | |
| B. | 22.4 L H2O所含的分子数为NA | |
| C. | NA个氢原子的质量为2 g | |
| D. | 1 mol NaCl中含0.5NA个Na+和0.5NA个Cl- |