题目内容
7.下列实验操作正确的是( )| A. | 用pH试纸测定新制氯水的pH=2 | |
| B. | 用玻璃棒在过滤器上搅拌以加速硫酸铜晶体的洗涤 | |
| C. | 向某溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀生成,则该溶液中不一定含有SO${\;}_{4}^{2-}$ | |
| D. | 向可溶性淀粉溶液中滴加碘酒,溶液呈蓝色,用CCl4作萃取剂振荡、静置后,下层呈紫红色 |
分析 A.氯水具有漂白性,无法用pH试纸测定氯水的pH;
B.在过滤器上搅拌,易导致滤纸受损;
C.生成的白色沉淀可能为氯化银,原溶液中可能含有银离子,不一定含有硫酸根离子;
D.碘单质易溶于四氯化碳,结合四氯化碳的密度大于水判断.
解答 解:A.氯水具有强氧化性,能够漂白试纸,则无法用pH试纸测定新制氯水的pH=2,故A错误;
B.过滤时,不能用玻璃棒搅拌,否则可能捣破滤纸,故B错误;
C.向某溶液中加入盐酸酸化的BaCl2溶液,有白色沉淀生成,该沉淀可能为AgCl,不一定为硫酸钡,故C正确;
D.向可溶性淀粉溶液中滴加碘酒,淀粉遇到碘单质呈蓝色,溶液中不存在碘单质,则用CCl4作萃取剂振荡、静置后,下层呈紫红色,故D错误;
故选c.
点评 本题考查了化学实验方案的设计与评价,题目难度不大,涉及氯水性质、pH试纸的使用方法、过滤、萃取、常见离子的检验等知识,明确常见化学实验基本操作方法为解答关键,试题培养了学生的化学实验能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.下列不属于有机物的是( )
| A. |  | B. | C6H6 | C. | CCl4 | D. |  |
18.如图所示的实验,能达到实验目的是( )
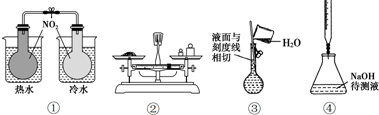

| A. | ①验证温度对平衡移动的影响 | B. | ②称量5.120gNaCl固体 | ||
| C. | ③配制一定物质的量浓度NaCl溶液 | D. | ④中和滴定 |
15.现有部分短周期元素的性质或原子结构如下表:
(1)写出A元素在周期表中的位置第三周期第ⅥA族.
(2)写出C元素气态氢化物的电子式 .
.
(3)元素D与元素A相比,非金属性较强的是Cl(用元素符号表示),下列表述中 能证明这一事实的是b(填选项序号).
a.常温下D的单质和A的单质状态不同 b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
(4)探寻物质的性质差异性是学习的重要方法之一.A、B、C、D四种元素的最高价氧化物 的水化物中化学性质明显不同于其他三种酸的是H2CO3(写化学式).
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,且K、M层电子数之和等于L层电子数 |
| B | 最外层电子数是次外层电的2倍 |
| C | 常温下单质为双原子分子,其氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
(2)写出C元素气态氢化物的电子式
 .
.(3)元素D与元素A相比,非金属性较强的是Cl(用元素符号表示),下列表述中 能证明这一事实的是b(填选项序号).
a.常温下D的单质和A的单质状态不同 b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
(4)探寻物质的性质差异性是学习的重要方法之一.A、B、C、D四种元素的最高价氧化物 的水化物中化学性质明显不同于其他三种酸的是H2CO3(写化学式).
2.下列有关H2O2跟H2SO4酸化的KMnO4溶液反应的化学方程式正确的是( )
| A. | 2KMnO4+H2O2+3H2SO4=K2SO4+2MnSO4+4H2O+3O2↑ | |
| B. | 2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+6H2O+4O2↑ | |
| C. | 2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+8H2O+5O2↑ | |
| D. | 2KMnO4+7H2O2+3H2SO4=K2SO4+2MnSO4+10H2O+6O2↑ |
6.下列各组物质间的转化关系正确的是( )
| A. | FeCl2(aq)$\stackrel{Cl_{2}}{→}$FeCl3(aq)$\stackrel{Cu}{→}$FeCl2(aq) | B. | H2SO3$\stackrel{△}{→}$Si02$\stackrel{HCl}{→}$SiCl4 | ||
| C. | NaCl(aq)$\stackrel{CO_{2}}{→}$NaHC03(s)$\stackrel{△}{→}$Na2CO3(s) | D. | CuS04 $\stackrel{NaOH(aq)}{→}$Cu(OH)2$→_{△}^{乙醛}$Cu |
7.试预测下列哪些物质不具备漂白性( )
| A. | 氯水 | B. | (CaCl2)氯化钙溶液 | ||
| C. | 漂白粉溶液 | D. | (NaClO)次氯酸钠溶液 |
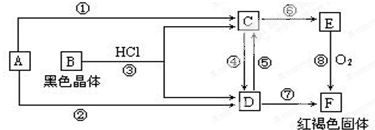
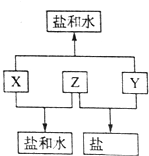 已知:A、B、C、D四种短周期元素,A与D原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,已知Z是常见的两性氢氧化物,试推断回答下列问题.
已知:A、B、C、D四种短周期元素,A与D原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,已知Z是常见的两性氢氧化物,试推断回答下列问题.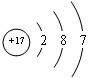 ;
;