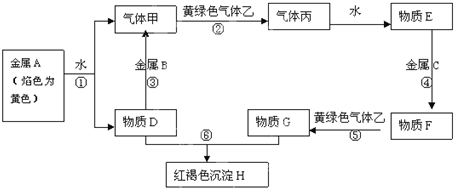
题目内容
3.下列各组离子因发生氧化还原反应而不能大量共存的是( )| A. | H+、Na+、S2-、Cl- | B. | OH-、ClO-、SO42-、S2- | ||
| C. | H+、MnO4-、Cl-、K+ | D. | K+、NO3-、Cl-、Fe2+ |
分析 A.氢离子与硫离子发生反应生成硫化氢气体,该反应不是氧化还原反应;
B.次氯酸根离子具有强氧化性,能够氧化硫离子;
C.酸性高锰酸根离子具有强氧化性,能够将氯离子氧化成氯气;
D.四种离子之间不发生反应,能够共存.
解答 解:A.H+、S2-之间反应生成硫化氢,在溶液中不能大量共存,但不是因发生氧化还原反应而不能大量共存,故A错误;
B.ClO-、S2-之间发生氧化还原反应,在溶液中不能大量共存,故B正确;
C.H+、MnO4-、Cl-之间发生氧化还原反应在溶液中不能大量共存,故C正确;
D.K+、NO3-、Cl-、Fe2+之间不反应,在溶液中能够大量共存,故D错误;
故选BC.
点评 本题考查离子共存的判断,为高考中的高频题,属于中等难度的试题,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
13.在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是( )
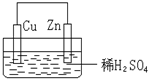

| A. | 铜片为负极 | B. | 锌片为负极 | ||
| C. | 电子通过导线由铜片流向锌片 | D. | 铜片上没有有H2逸出 |
15.一定量的Na2O2与CO2反应后的固体物质41.8g,恰好与1L 1mol•L-1的稀盐酸完全反应,下列说法正确的是( )
| A. | 41.8g固体物质为Na2CO3 | |
| B. | 41.8g固体物质为0.1mol Na2CO3和0.4mol Na2O2的混合物 | |
| C. | 41.8g固体物质为31.2g NaHCO3和10.6g Na2CO3的混合物 | |
| D. | 一定量的Na2O2为78g |
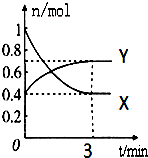 在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2 (g) (红棕色)?N2O4g)(无色),如图所示.
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2 (g) (红棕色)?N2O4g)(无色),如图所示.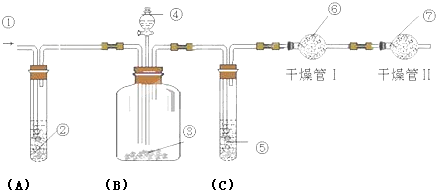
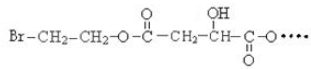
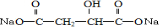 BHOCH2CH2OHC
BHOCH2CH2OHC D
D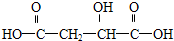
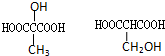
 .
. .
.
 ;
;