题目内容
13.在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是( )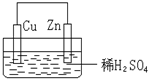
| A. | 铜片为负极 | B. | 锌片为负极 | ||
| C. | 电子通过导线由铜片流向锌片 | D. | 铜片上没有有H2逸出 |
分析 铜锌原电池中,Zn为负极,Cu为正极,负极发生氧化反应,正极发生还原反应,电子由负极流向正极,以此来解答.
解答 解:A.Zn失去电子,为负极,故A错误;
B.Zn失去电子,为负极,故B正确;
C.电子由Zn片通过导线流向Cu片,故C错误;
D.Cu电极上氢离子得到电子生成氢气,有氢气逸出,故D错误;
故选B.
点评 本题考查铜锌原电池,把握原电池的工作原理为解答的关键,注重基础知识的考查,注意电池反应为Zn与硫酸反应,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
3.一定条件下,在某容积固定的密闭容器中进行反应:2SO2(g)+O2(g)?2SO3(g),下列说法中,可以说明反应达到化学平衡状态的是( )
| A. | SO2、O2、SO3共存 | |
| B. | SO2、O2、SO3的总质量保持不变 | |
| C. | SO2、O2、SO3的物质的量浓度不再发生变化 | |
| D. | 以SO2表示的正反应和逆反应速率相等,且等于零 |
4.设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 1molCl2与足量Fe反应转移电子数一定为3NA | |
| B. | 标准状况下,22.4L NH3中含有共价键的数目为NA | |
| C. | 1.0L 1.0mol•L-1的Na2SiO3水溶液中含有的氧原子数为3NA | |
| D. | 4.6g Na完全转化成NaO和Na2O2的混合物,混合物中阴离子总数为0.1NA |
1.下列有关实验的操作、原理和现象,不正确的是( )
| A. | 纸上层析法通常以滤纸作为惰性支持物.滤纸纤维上的羟基具有亲水性,它所吸附的水作固定相 | |
| B. | 重结晶时,溶质的溶解度越大、溶液冷却速度越慢,得到的晶体颗粒越大 | |
| C. | 制备硫酸亚铁铵晶体需要将饱和硫酸铵溶液与新制硫酸亚铁溶液混合,加热蒸发,趁热过滤 | |
| D. | 在牙膏的浸泡液中加入新制碱性Cu(OH)2,溶液变绛蓝色 |
8.下列关于晶体的说法中,不正确的是( )
①晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性
②含有金属阳离子的晶体一定是离子晶体
③共价键可决定分子晶体的熔、沸点
④晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列.
①晶体中原子呈周期性有序排列,有自范性;而非晶体中原子排列相对无序,无自范性
②含有金属阳离子的晶体一定是离子晶体
③共价键可决定分子晶体的熔、沸点
④晶胞是晶体结构的基本单元,晶体内部的微粒按一定规律作周期性重复排列.
| A. | ①② | B. | ②④ | C. | ①④ | D. | ②③ |
18.如图所示装置的气密性检查中,一定漏气的是( )
| A. | 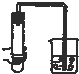 | B. |  | C. |  | D. | 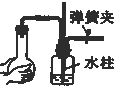 |
5.1mol某烃最多能和1molHCl发生加成反应,生成1mol氯代烷,1mol此氯代烷能和Cl2发生取代反应最多生成9molHCl,生成只含碳元素和氢元素的氯代烷,该烃可能是( )
| A. | CH3CH═CHCH2CH3 | B. | CH2═CHCH═CH2 | C. | CH2═CHCH3 | D. | CH3-CH═CH-CH3 |
2.能正确表示下列反应的离子方程式是( )
| A. | 过氧化钠固体与水反应:2O${\;}_{2}^{2-}$+2H2O═4OH-+O2↑ | |
| B. | 实验室制Fe(OH)3胶体:Fe3++3OH-═Fe(OH)3(胶体) | |
| C. | 向澄清石灰水中通入过量CO2:OH-+CO2═HCO3- | |
| D. | 将0.1mol/L的NH4Al(SO4)2溶液与0.3mol/L的Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
3.下列各组离子因发生氧化还原反应而不能大量共存的是( )
| A. | H+、Na+、S2-、Cl- | B. | OH-、ClO-、SO42-、S2- | ||
| C. | H+、MnO4-、Cl-、K+ | D. | K+、NO3-、Cl-、Fe2+ |