题目内容
15.美日三位科学家曾因对“有机物合成过程中钯催化交叉偶联”的研究获诺贝尔化学奖.评审委员会认定这项研究成果可以大大提升合成复杂化学物质的可能性.钯的化合物氯化钯可用来检测有毒气体CO,发生反应的化学方程式为:CO+PdCl2+H2O═CO2+Pd↓+2HC1.对该反应的下列说法正确的是( )| A. | CO作氧化剂,具有氧化性 | |
| B. | HCl是还原产物 | |
| C. | 反应中H2O提供了氧原子,因此H2O是氧化剂 | |
| D. | 生成22.4 L CO2(标准状况)时,转移的电子数为2NA |
分析 CO+PdCl2+H2O=CO2+Pd↓+2HCl中,C元素的化合价由+2价升高为+4价,Pb元素的化合价由+2降低为0,结合元素化合价的变化解答该题.
解答 解:CO+PdCl2+H2O=CO2+Pd↓+2HCl中,C元素的化合价由+2价升高为+4价,Pb元素的化合价由+2降低为0,
A.C元素的化合价升高,CO为还原剂,具有还原性,故A错误;
B.Pb元素的化合价由+2降低为0,反应中PbCl2被还原,Pb为还原产物,HCl为生成物,故B错误;
C.H、O元素的化合价均不变,水不是氧化剂,故C错误;
D.生成22.4 L CO2(标准状况)时,由C元素的化合价变化可知转移的电子数为$\frac{22.4L}{22.4L/mol}$×(4-2)×NA=2NA,故D正确;
故选D.
点评 本题考查氧化还原反应及计算,侧重于学生的分析与计算能力的考查,明确反应中元素的化合价变化及基本概念即可解答,题目难度不大.

练习册系列答案
相关题目
20.下列有关同分异构体数目的叙述中,不正确的是( )
| A. | 甲苯苯环上的一个氢原子被含4个碳原子的烷基取代,所得产物有12种 | |
| B. | 苯乙烯(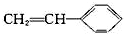 )和氢气完全加成的产物的一溴取代物有5种 )和氢气完全加成的产物的一溴取代物有5种 | |
| C. | 已知二氯苯有3种同分异构体,则四氯苯的同分异构体的数目为3种 | |
| D. | 相对分子质量为106.5的一氯代烃,有8种同分异构体 |
7.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 28g氮气所含有的原子数目为NA | |
| B. | 标准状况下,22.4L水中含有个水分子NA | |
| C. | 2NA个氯气的体积是NA个氧气的体积的2倍 | |
| D. | 标准状况下,22.4L氯化氢所含的原子数为2NA |
4.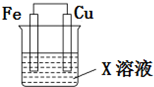 选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、铁棒、铜棒、铂棒,组成如图所示的原电池装置(只有两个电极),观察到电流计G的指针均明显偏转(指针偏转程度大),则其可能的组合共有( )
选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、铁棒、铜棒、铂棒,组成如图所示的原电池装置(只有两个电极),观察到电流计G的指针均明显偏转(指针偏转程度大),则其可能的组合共有( )
 选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、铁棒、铜棒、铂棒,组成如图所示的原电池装置(只有两个电极),观察到电流计G的指针均明显偏转(指针偏转程度大),则其可能的组合共有( )
选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、铁棒、铜棒、铂棒,组成如图所示的原电池装置(只有两个电极),观察到电流计G的指针均明显偏转(指针偏转程度大),则其可能的组合共有( )| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
5. 如图为氢氧燃料电池原理示意图,已知该燃料电池总反应为:2H2+O2═2H2O,a极反应为:H2+2OH--2e-═2H2O,下列叙述不正确的是( )
如图为氢氧燃料电池原理示意图,已知该燃料电池总反应为:2H2+O2═2H2O,a极反应为:H2+2OH--2e-═2H2O,下列叙述不正确的是( )
 如图为氢氧燃料电池原理示意图,已知该燃料电池总反应为:2H2+O2═2H2O,a极反应为:H2+2OH--2e-═2H2O,下列叙述不正确的是( )
如图为氢氧燃料电池原理示意图,已知该燃料电池总反应为:2H2+O2═2H2O,a极反应为:H2+2OH--2e-═2H2O,下列叙述不正确的是( )| A. | a电极是负极,发生氧化反应 | |
| B. | b电极的电极反应为4OH--4e-═2H2O+O2↑ | |
| C. | 氢氧燃料电池是一种具有应用前景的绿色电源 | |
| D. | 燃料电池内部H+从负极移向正极 |
 ,则合成涤纶的反应方程式和反应类型分别是
,则合成涤纶的反应方程式和反应类型分别是 、缩聚反应.
、缩聚反应.
 .
.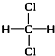 和
和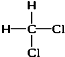
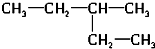 和
和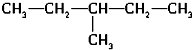 ⑦CH2=CH-CH2CH3和 CH3-CH=CH-CH3.
⑦CH2=CH-CH2CH3和 CH3-CH=CH-CH3.