题目内容
7.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )| A. | 28g氮气所含有的原子数目为NA | |
| B. | 标准状况下,22.4L水中含有个水分子NA | |
| C. | 2NA个氯气的体积是NA个氧气的体积的2倍 | |
| D. | 标准状况下,22.4L氯化氢所含的原子数为2NA |
分析 A.根据n=$\frac{m}{M}$计算出氮气的物质的量,然后可得出含有N原子数目;
B.标准状况下,水的状态不是气态;
C.没有指出在相同条件下,无法比较二者的体积大小;
D.根据n=$\frac{V}{{V}_{m}}$计算出含有氯化氢的物质的量及含有原子的数目.
解答 解:A.28g氮气的物质的量为:$\frac{28g}{28g/mol}$=1mol,1mol氮气分子中含有2molN原子,含有的原子数目为2NA,故A错误;
B.标准状况下,水不是气体,不能使用标准状况下的气体摩尔体积计算,故B错误;
C.不是相同条件下,气体摩尔体积不一定相同,则无法比较两种气体的体积大小,故C错误;
D.标准状况下,22.4L氯化氢的物质的量为:$\frac{22.4L}{22.4L/mol}$=1mol,1molHCl分子中含有2mol原子,所含的原子数为2NA,故D正确;
故选D.
点评 本题考查了物质的量的计算,题目难度不大,明确标准状况下气体摩尔体积的使用条件为解答关键,注意掌握物质的量与摩尔质量、阿伏伽德罗常数之间的关系,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
18.利用如图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 |  |
| A | 稀硝酸 | Na2S | AgNO3与 AgCl的浊液 | Ksp(AgCl)>Ksp(Ag2S) | |
| B | 浓硫酸 | 无水 乙醇 | 溴水 | 有乙烯生成 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性钡盐均可以生成白色沉淀 | |
| D | 稀硫酸 | Na2CO3 | Na2SiO3 溶液 | 酸性: 稀硫酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
15.美日三位科学家曾因对“有机物合成过程中钯催化交叉偶联”的研究获诺贝尔化学奖.评审委员会认定这项研究成果可以大大提升合成复杂化学物质的可能性.钯的化合物氯化钯可用来检测有毒气体CO,发生反应的化学方程式为:CO+PdCl2+H2O═CO2+Pd↓+2HC1.对该反应的下列说法正确的是( )
| A. | CO作氧化剂,具有氧化性 | |
| B. | HCl是还原产物 | |
| C. | 反应中H2O提供了氧原子,因此H2O是氧化剂 | |
| D. | 生成22.4 L CO2(标准状况)时,转移的电子数为2NA |
2.在锌与盐酸反应的实验中,甲同学得到的结果如表所示:
按要求回答下列问题:
(1)温度对该反应速率的影响规律为温度越高,反应速率越快.
(2)对比结果B与F,F速率明显快的原因是粉末状的锌粉与酸接触面积大,反应速率快.
(3)乙同学将表面积相同、纯度相同、体积也相同的同种锌片分别投入等体积、浓度不同的稀硫酸和稀盐酸中(两酸中的氢离子浓度相同),仔细观察后发现,投入到稀硫酸中的锌表面产生的气泡没有投入到稀盐酸的快,产生这一现象可能的原因是:硫酸根离子可能是这一反应的负催化剂或氯离子可能是正催化剂.(只需回答一条即可)如何用实验来验证向锌和稀硫酸反应中加氯化锌若反应速率加快则证明氯离子是正催化剂,或向锌和稀盐酸反应中加硫酸锌溶液在反应中若反应速率减慢则说明硫酸根离子是负催化剂.
| 锌的质量(g) | 锌的形状 | 温度(℃) | 溶解于酸所需的时间(s) | |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | 50 |
| E | 2 | 薄片 | 45 | 25 |
| F | 2 | 粉末 | 15 | 5 |
(1)温度对该反应速率的影响规律为温度越高,反应速率越快.
(2)对比结果B与F,F速率明显快的原因是粉末状的锌粉与酸接触面积大,反应速率快.
(3)乙同学将表面积相同、纯度相同、体积也相同的同种锌片分别投入等体积、浓度不同的稀硫酸和稀盐酸中(两酸中的氢离子浓度相同),仔细观察后发现,投入到稀硫酸中的锌表面产生的气泡没有投入到稀盐酸的快,产生这一现象可能的原因是:硫酸根离子可能是这一反应的负催化剂或氯离子可能是正催化剂.(只需回答一条即可)如何用实验来验证向锌和稀硫酸反应中加氯化锌若反应速率加快则证明氯离子是正催化剂,或向锌和稀盐酸反应中加硫酸锌溶液在反应中若反应速率减慢则说明硫酸根离子是负催化剂.
12.用以下三种途径来制取相同质量的硝酸铜:
①铜与浓硝酸反应;
②铜与稀硝酸反应;
③铜先跟氧气反应生成氧化铜,氧化铜再跟稀硝酸反应.
以下叙述中正确的是( )
①铜与浓硝酸反应;
②铜与稀硝酸反应;
③铜先跟氧气反应生成氧化铜,氧化铜再跟稀硝酸反应.
以下叙述中正确的是( )
| A. | 消耗铜的物质的量相等 | B. | 消耗硝酸的物质的量相等 | ||
| C. | 消耗铜的物质的量是①>②>③ | D. | 消耗硝酸的物质的量是①>②>③ |
16.与 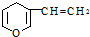 互为同分异构体的酚类化合物有( )
互为同分异构体的酚类化合物有( )
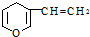 互为同分异构体的酚类化合物有( )
互为同分异构体的酚类化合物有( )| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
17.某实验室需要少量的一氯乙烷,下列制取方法中所得产物含量最高的是( )
| A. | 等物质的量的乙烷和氯气的光照反应 | |
| B. | 乙烯与氯气的加成反应 | |
| C. | 乙烯与氢气和氯气混合反应 | |
| D. | 乙烯与氯化氢加成反应 |
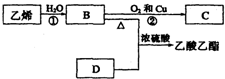 已知乙烯能发生以下转化:
已知乙烯能发生以下转化: