题目内容
17.对于反应2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O的说法不正确的是( )| A. | 该反应中,KMnO4是还原剂 | |
| B. | 该反应中,C元素被氧化 | |
| C. | 通过该反应可知,氧化性:KMnO4>CO2 | |
| D. | 该反应每转移1mol电子,同时生成1molCO2 |
分析 反应2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O中,Mn元素化合价降低,被还原,KMnO4为氧化剂,C元素化合价升高,被氧化,H2C2O4为还原剂,以此解答该题.
解答 解:A.Mn元素化合价降低,被还原,KMnO4为氧化剂,故A错误;
B.C元素化合价升高,被氧化,故B正确;
C.反应中KMnO4为氧化剂,H2C2O4为还原剂,生成CO2为氧化产物,所以根据氧化剂的氧化性大于氧化产物,则氧化性:KMnO4>CO2,故C正确;
D.C元素化合价由+3升高到+4,所以该反应每转移1mol电子,同时生成1molCO2,故D正确;
故选A.
点评 本题考查氧化还原反应,侧重于学生的分析能力和基本概念的理解和运用的考查,注意从元素化合价的角度认识相关概念及相关物质的性质的判断,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 工业上可用铝热反应大规模炼铁 | B. | SO2常用于纸张等植物纤维的漂白 | ||
| C. | Si是重要的半导体材料 | D. | 电解熔融MgCl2,可制得金属镁 |
8.反应A(g)+3B(g)═2C(g)+2D(g)在四种不同情况下的反应速率分别为
①v(A)=0.25mol/(L•s),
②v(B)=27mol/(L•min),
③v(C)=0.4mol/(L•s),
④v(D)=36mol/(L•min).
下列有关反应速率的比较中正确的是( )
①v(A)=0.25mol/(L•s),
②v(B)=27mol/(L•min),
③v(C)=0.4mol/(L•s),
④v(D)=36mol/(L•min).
下列有关反应速率的比较中正确的是( )
| A. | ④>②>③>① | B. | ①>④>②>③ | C. | ①>②>③>④ | D. | ④>①>③>② |
5.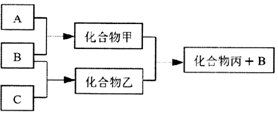 如图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成.其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子.下列说法错误的是( )
如图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成.其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子.下列说法错误的是( )
 如图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成.其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子.下列说法错误的是( )
如图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成.其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子.下列说法错误的是( )| A. | Z元素位于第二周期第VIA族 | |
| B. | 可用排水法收集化合物乙 | |
| C. | 元素X、Y、Z的原子半径大小关系为X<Z<Y | |
| D. | 化合物甲溶于化合物丙中,存在的微粒有5种 |
12.下列有关物质的分类不正确的是( )
| A. | 硫酸(酸) | B. | 溶液(混合物) | C. | Al2O3(两性氧化物) | D. | 纯碱(碱) |
2.下列有关物质的分离和提纯的方法中正确的是( )
| A. | 除去Cl2的HCl气体可以通过浓硫酸 | |
| B. | 碳酸钠固体中的碳酸氢钠杂质可以通过加热除去 | |
| C. | SO2可以通过碱石灰干燥 | |
| D. | FeCl3溶液中含有CuCl2可以加入足量NaOH溶液除去 |
9.下列有关化学用于正确的是( )
| A. | KCl的摩尔质量是:74.5g | B. | 一水合氨的化学式为:NH4•OH | ||
| C. | Na2O2中的阴离子为:O2- | D. | 镁的原子结构示意图如图所示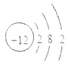 |
7.第二周期元素中,其基态原子未成对电子数最多为( )
| A. | 0 | B. | 1 | C. | 2 | D. | 3 |