题目内容
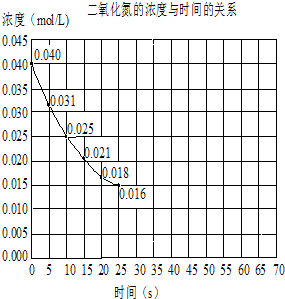 二氧化氮在加热条件下能够分解成一氧化氮和氧气.该反应进行到45s时,达到平衡NO2浓度约为0.0125mol/L.如图中的曲线表示二氧化氮分解反应在前25s内的反应进程.
二氧化氮在加热条件下能够分解成一氧化氮和氧气.该反应进行到45s时,达到平衡NO2浓度约为0.0125mol/L.如图中的曲线表示二氧化氮分解反应在前25s内的反应进程.(1)前20s内氧气的平均生成速率v(O2)为
(2)若反应延续至70s,请在图中用实线画出25s至70s的反应进程曲线.
(3)若在反应开始时加入催化剂(其他条件都不变),请在图上用虚线画出加入催化剂后的反应进程曲线.
考点:化学平衡建立的过程,反应速率的定量表示方法
专题:化学平衡专题
分析:(1)由图可知,20秒内NO2的浓度变化为0.04mol/L-0.018mol/L=0.022mol/L,根据v=
计算v(NO2),再利用速率之比等于化学计量数之比计算v(O2);
(2)该反应进行到45秒时,达到平衡是NO2浓度约为0.0125mol/L,据此画出25秒至70秒的反应进程曲线;
(3)若在反应开始时加入催化剂(其他条件都不变),反应速率加快,相同时间内NO2浓度变化量增大,到达平衡时间缩短,但不影响平衡移动,达到平衡是NO2浓度约为0.0125mol/L,据此用虚线画出加催化剂后的反应进程曲线.
| △c |
| △t |
(2)该反应进行到45秒时,达到平衡是NO2浓度约为0.0125mol/L,据此画出25秒至70秒的反应进程曲线;
(3)若在反应开始时加入催化剂(其他条件都不变),反应速率加快,相同时间内NO2浓度变化量增大,到达平衡时间缩短,但不影响平衡移动,达到平衡是NO2浓度约为0.0125mol/L,据此用虚线画出加催化剂后的反应进程曲线.
解答:
解:(1)由图可知,20秒内NO2的浓度变化为0.04mol/L-0.018mol/L=0.022mol/L,故v(NO2)
=0.0011mol/(L?s),对于2NO2?2NO+O2,速率之比等于化学计量数之比,所以v(O2)=
v(NO2)=
×0.0011mol/(L?s)=5.5×10-4mol/(L?s),
故答案为:前20秒内氧气的平均生成速率5.5×10-4mol/(L?s);
(2)该反应进行到45秒时,达到平衡是NO2浓度约为0.0125mol/L,据此用实线画出25秒至70秒的反应进程曲线为 ,
,
故答案为: ;
;
(3)若在反应开始时加入催化剂(其他条件都不变),反应速率加快,相同时间内NO2浓度变化量增大,到达平衡时间缩短,但不影响平衡移动,达到平衡是NO2浓度约为0.0125mol/L,据此用虚线画出加催化剂后的反应进程曲线为 ,
,
故答案为: ;
;
| 0.022mol/L |
| 20s |
| 1 |
| 2 |
| 1 |
| 2 |
故答案为:前20秒内氧气的平均生成速率5.5×10-4mol/(L?s);
(2)该反应进行到45秒时,达到平衡是NO2浓度约为0.0125mol/L,据此用实线画出25秒至70秒的反应进程曲线为
 ,
,故答案为:
 ;
;(3)若在反应开始时加入催化剂(其他条件都不变),反应速率加快,相同时间内NO2浓度变化量增大,到达平衡时间缩短,但不影响平衡移动,达到平衡是NO2浓度约为0.0125mol/L,据此用虚线画出加催化剂后的反应进程曲线为
 ,
,故答案为:
 ;
;
点评:考查化学平衡速率的有关计算、平衡常数、影响反应速率与平衡移动的因素等,难度中等,注意基础知识的理解掌握.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案
相关题目
“善待地球,科学发展,构建和谐”是“世界地球日”的主题.你认为下列行为不符的( )
| A、控制含磷洗涤剂的生产和使用,防止水体富营养化,保护水资源 |
| B、研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展 |
| C、开发太阳能、水能、风能、可燃冰等新能源、减少使用煤、石油等化石燃料 |
| D、实现资源的“3R”利用,即:减少资源消耗、增加资源的重复使用、资源的循环利用 |
《联合国气候变化框架公约》第十七次缔约方大会暨《京都议定书》第七次缔约方会议11月28日在南非港口城市德班召开.全世界各国要采取措施减少温室气体排放,低碳生活应从我做起.以下做法不能体现低碳生活的是( )
| A、注意节约用电 |
| B、尽量搭乘公共交通工具,减少私家车的使用 |
| C、减少食物加工过程 |
| D、大量使用薪柴为燃料 |
可逆反应①X(g)+2Y(g)?2Z(g)、②2M(g)?N(g)+p(g)分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板.反应开始和达到平衡状态是有关物理量的变化如图所示:
下列判断正确的是( )

下列判断正确的是( )
| A、反应①的正反应是吸热反应 | ||
| B、在平衡(I)和平衡(II)中的气体摩尔体积相同 | ||
C、达平衡(I)是X的体积分数为
| ||
| D、达平衡(I)时体系的压强与反应开始时体系的压强之比为10:11 |
食盐、食醋为家庭厨房中常用的调味品,利用这两种物质不能完成的实验是( )
| A、鉴别AgNO3溶液和BaCl2溶液 | ||
B、检验“洗厕净”中是否含有SO
| ||
| C、除去保温瓶内壁上的水垢 | ||
| D、检验鸡蛋壳(CaCO3)能否溶于酸 |
下列说法中正确的是( )
| A、可以利用BaCl2溶液来区分碳酸钾溶液和硫酸钾溶液 |
| B、22.4LO2中一定含有6.02×1023个氧分子 |
| C、在相同温度和压强下,相同体积的任何气体都含有相同数目的粒子 |
| D、0.5 molNaCl溶于0.5L水中得到的溶液的浓度是1.0mol/L |