题目内容
一块表面已部分氧化的钠的质量为0.77g,放入到10g水中后,得到氢气的质量是0.02g.求:
(1)钠和氧化钠的质量各是多少?
(2)所得溶液的溶质的质量分数是多少?(氧化钠和水反应生成氢氧化钠)
(1)钠和氧化钠的质量各是多少?
(2)所得溶液的溶质的质量分数是多少?(氧化钠和水反应生成氢氧化钠)
考点:有关混合物反应的计算,化学方程式的有关计算
专题:计算题
分析:(1)根据反应2Na+2H2O=2NaOH+H2↑计算样品中Na的质量,进而计算Na2O的质量;
(2)利用n=
计算Na、Na2O的物质的量,再利用钠元素守恒计算生成NaOH的总物质的量,根据m=nM计算氢氧化钠的质量,溶液质量=0.77g+10g-0.02g=10.75g,进而计算溶液质量分数.
(2)利用n=
| m |
| M |
解答:
解:(1)反应生成得到氢气的质量是0.02g,则
2Na+2H2O=2NaOH+H2↑
46g 2g
m(Na) 0.02g
m(Na)=
=0.46g,
m(Na2O)=0.77g-0.46g=0.31g,
答:金属钠样品中含金属钠质量是0.46g,氧化钠质量为0.31g;
(2)n(Na2O)=
=0.005mol,混合物中n(Na)=
=0.02mol,
根据钠元素守恒,与水反应生成的n(NaOH)=0.02mol+0.005mol×2=0.03mol,则n(NaOH)=0.03mol×40g/mol=1.2g,溶液质量=0.77g+10g-0.02g=10.75g,溶液质量分数为
×100%=11.16%,
答:所得溶液的溶质的质量分数是11.16%.
2Na+2H2O=2NaOH+H2↑
46g 2g
m(Na) 0.02g
m(Na)=
| 46g×0.02g |
| 2g |
m(Na2O)=0.77g-0.46g=0.31g,
答:金属钠样品中含金属钠质量是0.46g,氧化钠质量为0.31g;
(2)n(Na2O)=
| 0.31g |
| 62g/mol |
| 0.46g |
| 23g/mol |
根据钠元素守恒,与水反应生成的n(NaOH)=0.02mol+0.005mol×2=0.03mol,则n(NaOH)=0.03mol×40g/mol=1.2g,溶液质量=0.77g+10g-0.02g=10.75g,溶液质量分数为
| 1.2g |
| 10.75g |
答:所得溶液的溶质的质量分数是11.16%.
点评:本题考查混合物的计算、根据方程式的计算等,难度不大,注意根据Na元素质量守恒计算氢氧化钠.

练习册系列答案
 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
相关题目
在电解水制取H2和O2时,为了增强溶液的导电性,常常要加入一些电解质,最好选用下列物质中的( )
| A、HCl |
| B、MgSO4 |
| C、CuSO4 |
| D、NaCl |
100℃时,两种气态烃以任意比混合,1L混合烃与9L O2混合,充分燃烧后恢复到原状态,所得气体体积仍为10L.下列各组混合烃不符合此条件的是( )
| A、CH4和C2H4 |
| B、CH4和C3H4 |
| C、C2H2和C3H6 |
| D、C2H4和C3H4 |
钓鱼岛及其附属岛屿是中国的固有领土,我国历来十分重视海水资源的综合利用,下列有关海水综合利用的说法不正确的是( )
| A、从海带中提取碘单质的过程不涉及氧化还原反应 |
| B、往淡水中加入NaCl等配成人造海水,可用于海产品的长途运输 |
| C、赤潮主要是由工农业生产和生活废水引起沿海水域的富营养化而造成的 |
| D、虽然海水中元素的种类很多,总储量很大,但许多元素的富集程度很低 |
用如图所示实验装置进行相应实验,能达到实验目的是( )


| A、装置①可用于除去Cl2中含有的少量HCl气体 |
| B、按装置②所示的气流方向可用于收集H2、NH3等 |
| C、装置③可证明非金属性Cl>C>Si |
| D、装置④向左推动针筒活塞可检验该装置的气密性 |
下列下列化学用语正确的是( )
| A、三氯化铁溶液中加入铁粉Fe3++Fe═2Fe2+ |
B、过氧化钠电子式: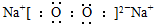 |
C、Na+结构简图: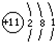 |
| D、少量氯气通入溴化亚铁溶液中2FeBr2+3Cl2═2FeCl3+2 Br2 |
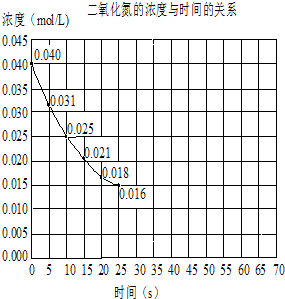 二氧化氮在加热条件下能够分解成一氧化氮和氧气.该反应进行到45s时,达到平衡NO2浓度约为0.0125mol/L.如图中的曲线表示二氧化氮分解反应在前25s内的反应进程.
二氧化氮在加热条件下能够分解成一氧化氮和氧气.该反应进行到45s时,达到平衡NO2浓度约为0.0125mol/L.如图中的曲线表示二氧化氮分解反应在前25s内的反应进程.