题目内容
16.将a g下列选项中的物质在足量的氧气中完全燃烧,再将产生的气体通过足量的Na2O2固体,充分反应后,固体增加的质量大于a g的是( )| A. | CO和H2 | B. | C6H12O6 | C. | CH2O2 | D. | C2H5OH |
分析 水、二氧化碳和Na2O2反应方程式分别为2H2O+2Na2O2=4NaOH+O2、2Na2O2+2CO2=2Na2CO3+O2,根据方程式知,水和Na2O2反应时固体质量增加量相当于H2质量,二氧化碳和Na2O2反应时固体质量增加量相当于CO质量,将可燃物写出H2或CO或(CO)m•Hn方式,如果恰好写为H2或CO或(CO)m•Hn方式,则产物通过足量Na2O2时固体质量不变,如果改写化学式时O原子有剩余,则反应前后固体质量减少,如果C原子有剩余,则固体质量增加,以此解答该题.
解答 解:A.通过以上分析知,可燃物是CO和氢气,在反应前后固体质量不变,不符合,故A不选;
B.该化学式可以改写为(CO)6•H12,则反应前后固体质量不变,不符合,故B不选;
C.该化学式可以改写为CO.H2.O,O原子有剩余,所以反应前后固体质量减少,不符合,故C不选;
D.该化学式可以改写为(CO)•3H2.C,则反应前后固体质量增大,符合,故D选.
故选D.
点评 本题考查化学方程式有关计算,明确反应前后固体质量增加成分是解本题关键,利用化学式分析判断即可,注意解题方法技巧,题目难度中等.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
14.以苯甲醛为原料,通过Cannizzaro反应来制备苯甲醇和苯甲酸,反应式为:
主反应:
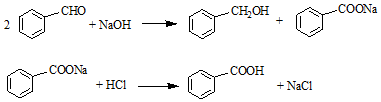
副反应:
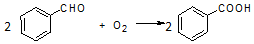
主要物料的物理常数如表:
实验步骤:
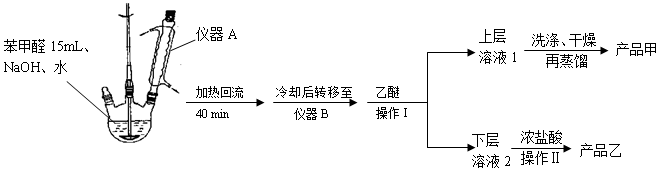
(1)仪器A的作用是冷凝回流.
(2)蒸馏操作时温度应该控制在205℃左右.获得产品乙时进行的操作Ⅱ的名称是抽滤(过滤、减压过滤).
(3)①上层溶液1中除乙醚外主要有机杂质是苯甲醛、苯甲酸.
洗涤时先后用到了饱和NaHSO3溶液、10%的NaHCO3溶液和水.
②洗涤操作在d中进行.
a.烧杯 b.布氏漏斗 c.烧瓶 d.分液漏斗
③加入10%的NaHCO3溶液至无气泡生成(填现象)时说明杂质已被除尽.
(4)若产品甲的质量为5.40g,则产品甲的产率是66.7%.
主反应:

副反应:
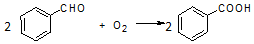
主要物料的物理常数如表:
| 名称 | 分子量 | 性状 | 相对密度 (g•cm-3) | 沸点 (℃) | 溶解度 | ||
| 水 | 乙醚 | ||||||
| 苯甲醛 | 106 | 无色液体 | 1.04 | 179 | 微溶 | 易溶 | |
| 苯甲酸 | 122 | 无色晶体 | 1.27 | 249 | 0.21g | 66g | |
| 苯甲醇 | 108 | 无色液体 | 1.04 | 205 | 微溶 | 易溶 | |
| 乙醚 | 74 | 无色液体. | 0.71 | 35 | 不溶 | -- | |

(1)仪器A的作用是冷凝回流.
(2)蒸馏操作时温度应该控制在205℃左右.获得产品乙时进行的操作Ⅱ的名称是抽滤(过滤、减压过滤).
(3)①上层溶液1中除乙醚外主要有机杂质是苯甲醛、苯甲酸.
洗涤时先后用到了饱和NaHSO3溶液、10%的NaHCO3溶液和水.
②洗涤操作在d中进行.
a.烧杯 b.布氏漏斗 c.烧瓶 d.分液漏斗
③加入10%的NaHCO3溶液至无气泡生成(填现象)时说明杂质已被除尽.
(4)若产品甲的质量为5.40g,则产品甲的产率是66.7%.
7.把0.1mol KOH固体分别加入到下列100ml的液体中,溶液的导电能力无变化的是( )
| A. | 纯净水 | B. | 0.lmol/LHCl | C. | 1.0mol/LCH3COOH | D. | 0.5mol/LH2SO4 |
4.下列氧化还原反应中,水作为氧化剂的是( )
| A. | C+H2O $\frac{\underline{\;高温\;}}{\;}$CO+H2 | B. | 3NO2+H2O=2HNO3+NO | ||
| C. | Cl2+SO2+H2O=H2SO4+2HCl | D. | 2F2+2H2O=4HF+O2 |
11.在粗碘中含ICl和IBr,受热时I2、ICl、IBr均可升华,在粗碘中加入一种物质后,再进行升华可制得精碘,应加入的物质是( )
| A. | H2O | B. | Zn | C. | KCl | D. | KI |
1.向含有amol FeBr2的溶液中,通入x mol Cl2,下列各项为通Cl2过程中,溶液发生反应的离子方程式,其中正确的是( )
| A. | x=0.6a 2Fe2++Cl2=2Fe3++2Cl- | |
| B. | x=a 2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- | |
| C. | x=0.4a 2Br-+Cl2=Br2+2Cl- | |
| D. | x=2a 2Fe2++6Br-+4Cl2=3Br2+2Fe3++8Cl- |
5.用下列装置进行的实验,能达到相应实验目的是( )
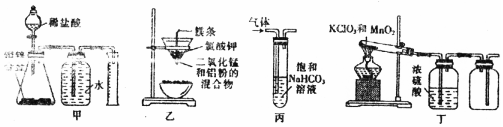

| A. | 装置甲:测定合金中Zn的含量 | B. | 装置乙:制取金属锰 | ||
| C. | 装置丙:洗气除去SO2中的CO2 | D. | 装置丁:实验室制取O2 |
6.下列说法不能说明H3PO4的酸性弱于H2SO4的是( )
| A. | 非金属性P<S | |
| B. | H3PO4溶液的导电能力弱于H2SO4溶液 | |
| C. | Na3PO4溶液呈碱性,Na2SO4溶液呈中性 | |
| D. | H2SO4溶液与Na3PO4反应可以生成H3PO4和Na2SO4 |
 向100mL 3mol•L-1硫酸铝铵【NH4Al(SO4)2】溶液中逐滴加入1mol•L-1Ba(OH)2溶液.
向100mL 3mol•L-1硫酸铝铵【NH4Al(SO4)2】溶液中逐滴加入1mol•L-1Ba(OH)2溶液.