题目内容
下列离子方程式正确的是( )
| A、氯气通入水中:Cl2+H2O=2H++Cl-+ClO- |
| B、向Fe(OH)3中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| C、向Fe(NO3)2稀溶液中加入盐酸:Fe2++4H++NO3-=Fe3++NO↑+2H2O |
| D、向NaHCO3溶液中加入少量的Ba(OH)2溶液:Ba2++2HCO3-+2OH-=BaCO3↓+CO32-+2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A、次氯酸是弱电解质不能拆成离子;
B、铁离子具有氧化性能氧化碘离子为碘单质;
C、选项中电荷不守恒;
D、酸式盐和碱反应量少的全部反应,离子方程式中符合化学式组成比.
B、铁离子具有氧化性能氧化碘离子为碘单质;
C、选项中电荷不守恒;
D、酸式盐和碱反应量少的全部反应,离子方程式中符合化学式组成比.
解答:
解:A、次氯酸是弱电解质不能拆成离子,氯气通入水中的离子方程式:Cl2+H2O=H++Cl-+HClO,故A错误;
B、铁离子具有氧化性能氧化碘离子为碘单质,向Fe(OH)3中加入氢碘酸反应的离子方程式:2Fe(OH)3+2I-+6H+=2Fe2++6H2O+I2,故B错误;
C、选项中电荷不守恒,向Fe(NO3)2稀溶液中加入盐酸反应的离子方程式:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O,故C错误;
D、酸式盐和碱反应量少的全部反应,离子方程式中符合化学式组成比,向NaHCO3溶液中加入少量的Ba(OH)2溶液:Ba2++2HCO3-+2OH-=BaCO3↓+CO32-+2H2O,故D正确;
故选D.
B、铁离子具有氧化性能氧化碘离子为碘单质,向Fe(OH)3中加入氢碘酸反应的离子方程式:2Fe(OH)3+2I-+6H+=2Fe2++6H2O+I2,故B错误;
C、选项中电荷不守恒,向Fe(NO3)2稀溶液中加入盐酸反应的离子方程式:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O,故C错误;
D、酸式盐和碱反应量少的全部反应,离子方程式中符合化学式组成比,向NaHCO3溶液中加入少量的Ba(OH)2溶液:Ba2++2HCO3-+2OH-=BaCO3↓+CO32-+2H2O,故D正确;
故选D.
点评:本题考查了离子方程式书写方法和注意问题,主要是弱电解质判断,氧化还原反应分析,酸式盐和碱反应量少的全部反应,题目难度中等.

练习册系列答案
相关题目
下列说法或表示方法正确的是( )
A、丙烷分子的比例模型: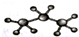 |
| B、乙醚的分子式为:C2H6O |
C、2-乙基-1,3-丁二烯分子的键线式: |
| D、化学名词:乙酸乙脂、苯、活性碳、钳锅 |
根据下表中烃的分子式排列规律,空格中烃的同分异构体中一氯代物种数不可能是( )
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |
| A、1种 | B、2种 | C、3种 | D、4种 |
下列分离、提纯、鉴别物质的方法正确的是( )
| A、用加热、蒸发的方法可以除去粗盐中的CaCl2、MgCl2杂质 |
| B、用渗析的方法除去NaCl溶液中含有的少量淀粉胶体 |
| C、用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
| D、用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 |
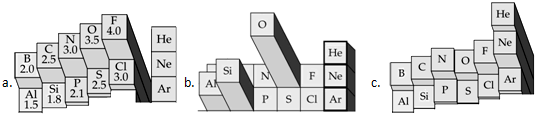
A、B、C均为短周期元素,它们在周期表中的位置如图所示.B、C两元素原子序数之和为A元素原子序数的4倍,则A、B、C依次是( )
| A | ||
| B | C |
| A、C、Al、P |
| B、N、Si、S |
| C、O、P、Cl |
| D、F、S、Ar |
下列反应的离子方程式正确的是( )
| A、氨气通入醋酸溶液CH3COOH+NH3═CH3COONH4 |
| B、金属钠跟水反应Na+H2O═Na++OH-+H2↑ |
| C、碳酸钡溶于醋酸BaCO3+2H+═Ba2++H2O+CO2↑ |
| D、澄清的石灰水跟盐酸反应H++OH-═H2O |
为测定某有机物的结构,用核磁共振仪处理后得到如图所示的核磁共振氢谱,则该有机物可能是( )
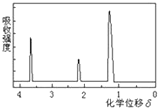

| A、C2H5OH |
B、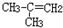 |
| C、CH3CH2CH2COOH |
D、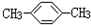 |
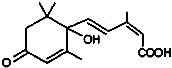 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开,S-诱抗素的 分子结构如图,下列关于该分子的说法中正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开,S-诱抗素的 分子结构如图,下列关于该分子的说法中正确的是( )| A、含有碳碳双键、羟基、羰基、羧基 |
| B、能发生加成反应、氧化反应、取代反应、缩聚反应 |
| C、1mol该分子能与含2mol NaOH的溶液完全反应 |
| D、该分子能与溴水反应而使溴水褪色且1mol它能与溴水中的4mol Br2反应 |