题目内容
 微型纽扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-═ZnO+H2O,Ag2O+H2O+2e-═2Ag+2OH-.下列叙述正确的是( )
微型纽扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-═ZnO+H2O,Ag2O+H2O+2e-═2Ag+2OH-.下列叙述正确的是( )| A、在使用过程中,电解质KOH被不断消耗 |
| B、使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C、每转移2mol e-,有232gAg2O被氧化 |
| D、Zn是负极,Ag2O是正极 |
考点:化学电源新型电池
专题:
分析:银锌电池的电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e=ZnO+H2O;Ag2O+H2O+2e=2Ag+2OH-,则Zn为负极,发生氧化反应,Ag2O为正极,发生还原反应,电子由负极流向正极,以此来解答.
解答:
解:A. 根据总反应:Ag2O+Zn═2Ag+ZnO,在使用过程中,电解质KOH没有被消耗,故A错误;
B、Zn为负极,Ag2O为正极,电流由正极经外电路流向负极,故B错误;
C、正极反应为Ag2O+H2O+2e=2Ag+2OH-,外电路中每通过2mol电子,则有232gAg2O被还原,故C错误;
D、Zn电极为负极发生氧化反应,Ag2O电极为正极发生还原反应,故D正确;
故选D.
B、Zn为负极,Ag2O为正极,电流由正极经外电路流向负极,故B错误;
C、正极反应为Ag2O+H2O+2e=2Ag+2OH-,外电路中每通过2mol电子,则有232gAg2O被还原,故C错误;
D、Zn电极为负极发生氧化反应,Ag2O电极为正极发生还原反应,故D正确;
故选D.
点评:本题考查原电池的工作原理,为高频考点,侧重学生的分析能力的考查,明确电极反应、正负极的判断、电子的流向即可解答,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
实验室中,下列除去括号内杂质的有关操作正确的是( )
| A、苯(硝基苯):加少量蒸馏水振荡,待分层后分液 |
| B、乙醇(水):加新制的生石灰,蒸馏 |
| C、CO2(HCl、水蒸气):通过盛有碱石灰的干燥管 |
| D、乙烷(乙烯):通入氢气发生加成反应 |
浓度均为0.1mol/L的下列溶液,pH最大的是( )
| A、HCl溶液 |
| B、NaHCO3溶液 |
| C、K2CO3溶液 |
| D、Cu(NO3)2溶液 |
下列叙述正确的是( )
| A、放热反应在任何温度下均能自发进行 |
| B、自发过程指的是常温下,不借助外力就能自动进行的过程 |
| C、熵增加的放热反应在任何温度下均能自发进行 |
| D、对于同一物质,其熵值大小为S(g)<S(l)<S(s) |
 用气体传感器可以检测汽车尾气中CO的含量.传感器是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法正确的是( )
用气体传感器可以检测汽车尾气中CO的含量.传感器是以燃料电池为工作原理,其装置如图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质NASICON中自由移动.下列说法正确的是( )| A、燃料电池工作时,电极b作负极 |
| B、工作时,电流由负极通过传感器流向正极 |
| C、b电极的电极反应式为:O2+2H2O+4e-═4OH- |
| D、当消耗11.2L(标准状况下)CO时,理论上传感器中会通过NA个电子 |
火法炼铜得到的粗铜中含多种杂质(如锌、金和银等),其性能远不能达到电气工业的要求,工业上常使用电解精炼法将粗铜提纯.在电解精炼时( )
| A、粗铜接电源负极 |
| B、纯铜作阳极 |
| C、杂质都将以单质形式沉积到池底 |
| D、纯铜片增重2.56g,电路中通过电子为0.08mol |
下列化学用语正确的是( )
A、
 | ||
B、某有机物的分子的简易球棍模型如图,分子式为C3H7O2N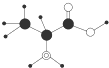 | ||
C、羟基乙酸(HOCH2COOH)的缩聚物: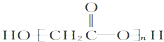 | ||
| D、铁在元素周期表中位于第4周期第ⅧB 族 |