题目内容
图Ⅰ是NO2(g)+CO(g)?CO2(g)+NO(g)反应过程中能量变化示意图.一定条件下,在固定容积的密闭容器中该反应达到平衡状态.当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ,下列有关说法正确的是( )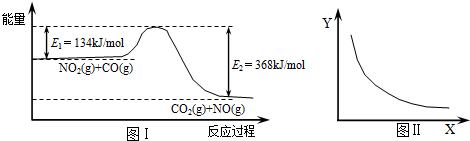

| A、该反应的焓变△H=+234 kJ?mol-1 |
| B、若X表示体系的压强,则Y表示的可能是NO2的转化率 |
| C、若X表示温度则Y表示的可能是CO2物质的量浓度 |
| D、增大CO的起始浓度,平衡向正反应方向移动,反应热增大 |
考点:化学平衡的影响因素,化学平衡建立的过程
专题:化学平衡专题
分析:A、反应的焓变=拆化学键吸收能量-形成化学键放出能量;
B、反应前后气体体积不变,压强的改变平衡不移动,二氧化氮的转化率不变;
C、反应是放热反应,温度升高反应逆向进行;
D、热化学方程式中反应热数值与化学计量数有关,与参加反应的反应物的物质的量无关.
B、反应前后气体体积不变,压强的改变平衡不移动,二氧化氮的转化率不变;
C、反应是放热反应,温度升高反应逆向进行;
D、热化学方程式中反应热数值与化学计量数有关,与参加反应的反应物的物质的量无关.
解答:
解:A、反应的焓变△H=E1-E2=134KJ/mol-368KJ/mol=-234kJ/mol,故A错误;
B、反应前后气体体积不变,压强的改变平衡不移动,二氧化氮的转化率不变,故B错误;
C、该反应是放热反应,升温,化学平衡逆向进行,二氧化碳浓度减小,故C正确;
D、反应放出的热量与参加反应的反应物的物质的量有关,但热化学方程式中反应热数值与化学计量数有关,与参加反应的反应物的物质的量无关,故反应热△H不变,故D错误;
故选C.
B、反应前后气体体积不变,压强的改变平衡不移动,二氧化氮的转化率不变,故B错误;
C、该反应是放热反应,升温,化学平衡逆向进行,二氧化碳浓度减小,故C正确;
D、反应放出的热量与参加反应的反应物的物质的量有关,但热化学方程式中反应热数值与化学计量数有关,与参加反应的反应物的物质的量无关,故反应热△H不变,故D错误;
故选C.
点评:本题考查了反应焓变的含义和计算,化学平衡的影响因素,反应物的转化率变化,主要是理解图象分析方法.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
对以下事实解释错误的是( )
| A、在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 |
| B、氢气可以在氯气中燃烧,说明燃烧反应未必需要氧气参与 |
| C、常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸根本就不会反应 |
| D、反应CuSO4+H2S→CuS↓+H2SO4能进行,说明CuS既不溶于水,也不溶于稀硫酸 |
设NA代表阿伏加德罗常数的值,下列说法中正确的是( )
| A、过氧化钠与水反应生成11.2L(标准状况下)氧气,反应中转移的电子数约为2NA |
| B、常温常压下,22.4L NO气体的分子数小于NA |
| C、常温常压下,0.5 mol?L-1的乙酸溶液中,乙酸分子的数目小于0.5NA |
| D、7.8 g Na2S和Na2O2的混合物中含有的阴离子数大于0.1 NA |
用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,下列实验操作会引起测定结果偏高的是:①用天平称量NaOH固体时,将NaOH放在右盘,砝码放在左盘,并移动游码使之平衡.②滴定前有气泡,滴定终点无气泡.③用蒸馏水洗净锥形瓶后盛入待测NaOH溶液进行滴定.④用蒸馏水洗净酸滴定管后盛入标准盐酸进行滴定.⑤滴定终点读取酸滴定管数据时,仰视刻度线.( )
| A、①⑤ | B、②④⑤ |
| C、②③④⑤ | D、①②③④⑤ |
用已知浓度的酸滴定未知浓度的碱时,会导致待测碱液的浓度偏低的操作是( )
①酸式滴定管用蒸馏水洗后,未用标准液润洗
②碱式滴定管用蒸馏水洗后,未用待测液润洗
③配制碱液时,称量的固体吸潮
④滴定前酸式滴定管尖嘴部分未充满溶液
⑤滴定中不慎将锥形瓶内液体摇出少量于瓶外.
①酸式滴定管用蒸馏水洗后,未用标准液润洗
②碱式滴定管用蒸馏水洗后,未用待测液润洗
③配制碱液时,称量的固体吸潮
④滴定前酸式滴定管尖嘴部分未充满溶液
⑤滴定中不慎将锥形瓶内液体摇出少量于瓶外.
| A、①③④ | B、②⑤ |
| C、②③⑤ | D、①③ |
丙烯醇(CH2═CH-CH2OH)可发生的化学反应有( )
①加成 ②氧化 ③燃烧 ④与钠反应.
①加成 ②氧化 ③燃烧 ④与钠反应.
| A、①②③ | B、②③④ |
| C、①②③④ | D、①③④ |
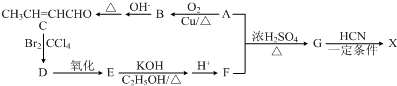
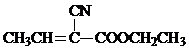 )是合成某种手术用粘合剂的单体,X的合成路线如图:
)是合成某种手术用粘合剂的单体,X的合成路线如图: