题目内容
8.有如下物质:(请用序号填空)A、稀硫酸 B、铜 C、金刚石 D、熔融NaCl E、NH3 F、Na2O G、酒精 H、SO3 I、HCl J、空气
(1)电解质:DFI;(2)非电解质EGH;(3)当前状况能导电ABD.
分析 电解质:在水溶液中或熔融状态下能导电的化合物;例:酸、碱、盐,金属氧化物等.非电解质:在水溶液中或熔融状态下不能导电的化合物;例:有机物,非金属氧化物等.
解答 解:A、稀硫酸能导电,属于混合物,既不是电解质也不是非电解质;
B、铜能导电,属于金属单质,既不是电解质也不是非电解质;
C、金刚石不能导电,属于非金属单质,既不是电解质也不是非电解质;
D、熔融NaCl能导电,属于盐,是电解质;
E、NH3 不能导电,溶于水导电的原因是氨气与水反应生成了一水合氨,氨气是非电解质;
F、Na2O不能导电,熔融状态下能导电,属于电解质;
G、酒精不能导电,属于非电解质;
H、SO3不能导电,溶于水导电的原因是三氧化硫与水反应生成了硫酸,硫酸属于电解质,三氧化硫是非电解质;
I、HCl不能导电,溶于水或熔融状态下能导电,属于电解质;
J、空气不能导电,属于混合物,既不是电解质也不是非电解质,故答案为:(1)DFI;(2)EGH;(3)ABD.
点评 本题考查了电解质、非电解质的判断,难度不大,根据定义判断即可,注意不是电解质的物质不一定是非电解质,如单质和混合物.

练习册系列答案
相关题目
19.某强酸性溶液X中可能含有Fe2+、Al3+、NH4+、CO32-、SO32-、SO42-、Cl-中的若干种,现取X溶液进行连续实验,实验过程及产物如下:
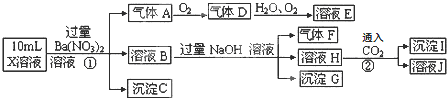
下列说法正确的是( )

下列说法正确的是( )
| A. | 气体F不能与溶液E发生反应 | |
| B. | X中肯定存在Fe2+、Al3+、NH4+、SO42- | |
| C. | X中肯定不存在CO32-、SO32-、Cl- | |
| D. | X中不能确定的离子是Al3+和Cl- |
16. 甲醇是重要的化工原料,又可做为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
甲醇是重要的化工原料,又可做为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
ⅠCO(g)+2H2(g)?CH3OH(g)△H1
ⅡCO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2=-58kJ/mol
ⅢCO2(g)+H2(g)?CO(g)+H2O(g)△H3
回答下列问题:
(1)物质的标准生成热是常用的化学热力学数据,可以用来计算化学反应热.即化学反应热:△H=生成物标准生成热综合-反应物标准生成热总和.
已知四种物质的标准生成热如表:
A.计算△H1=-90.73kJ/molkJ/mol B.△H3>0(填=、<、>)
(2)由甲醇在一定条件下制备甲醚.一定温度下,在三个体积均为1.0L的恒容密闭容器中发生反应:2CH3OH(g)?CH3OCH3(g)+H2O(g).实验数据见表:
下列说法正确的是AD
A.该反应的正反应为放热反应
B.达到平衡时,容器a中的CH3OH体积分数比容器b中的小
C.容器a中反应到达平衡所需时间比容器c中的长
D.若起始时向容器a中充入CH3OH 0.15mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
(3)合成气的组成$\frac{n({H}_{2})}{n(CO+C{O}_{2})}$=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图所示.
①α(CO)值随温度升高而减小(填“增大”或“减小”),其原因是升高温度时,反应Ⅰ为放热反应,平衡向左移动,使得体系中CO的量增大;反应Ⅲ为吸热反应,平衡向右移动,CO产生的量也增大;总结果,随温度升高,使CO的转化率降低.
②图中P1、P2、P3的大小关系为P3>P2>P1,其判断理由是相同温度下,由于反应Ⅰ为气体分子数减小的反应,加压有利于提升CO的转化率;而反应Ⅲ为气体分子数不变的反应,产生CO的量不受压强影响;故增大压强,CO的转化率升高.
(4)甲醇可以制成燃料电池,与合成气制成燃料电池相比优点是:装置简单,减小了电池的体积;若以硫酸作为电解质其负极反应为:CH3OH-6e-+H2O=CO2+6H+.
 甲醇是重要的化工原料,又可做为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
甲醇是重要的化工原料,又可做为燃料.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:ⅠCO(g)+2H2(g)?CH3OH(g)△H1
ⅡCO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2=-58kJ/mol
ⅢCO2(g)+H2(g)?CO(g)+H2O(g)△H3
回答下列问题:
(1)物质的标准生成热是常用的化学热力学数据,可以用来计算化学反应热.即化学反应热:△H=生成物标准生成热综合-反应物标准生成热总和.
已知四种物质的标准生成热如表:
| 物质 | CO | CO2 | H2 | CH3OH(g) |
| 标准生成热(kJ/mol) | -110.52 | -393.51 | 0 | -201.25 |
(2)由甲醇在一定条件下制备甲醚.一定温度下,在三个体积均为1.0L的恒容密闭容器中发生反应:2CH3OH(g)?CH3OCH3(g)+H2O(g).实验数据见表:
| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |||
| CH3OH(g) | CH3OCH3(g) | H2O(g) | CH3OCH3(g) | H2O(g) | ||
| a | 387 | 0.20 | 0 | 0 | 0.080 | 0.080 |
| b | 387 | 0.40 | 0 | 0 | ||
| c | 207 | 0.20 | 0 | 0 | 0.090 | 0.090 |
A.该反应的正反应为放热反应
B.达到平衡时,容器a中的CH3OH体积分数比容器b中的小
C.容器a中反应到达平衡所需时间比容器c中的长
D.若起始时向容器a中充入CH3OH 0.15mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
(3)合成气的组成$\frac{n({H}_{2})}{n(CO+C{O}_{2})}$=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图所示.
①α(CO)值随温度升高而减小(填“增大”或“减小”),其原因是升高温度时,反应Ⅰ为放热反应,平衡向左移动,使得体系中CO的量增大;反应Ⅲ为吸热反应,平衡向右移动,CO产生的量也增大;总结果,随温度升高,使CO的转化率降低.
②图中P1、P2、P3的大小关系为P3>P2>P1,其判断理由是相同温度下,由于反应Ⅰ为气体分子数减小的反应,加压有利于提升CO的转化率;而反应Ⅲ为气体分子数不变的反应,产生CO的量不受压强影响;故增大压强,CO的转化率升高.
(4)甲醇可以制成燃料电池,与合成气制成燃料电池相比优点是:装置简单,减小了电池的体积;若以硫酸作为电解质其负极反应为:CH3OH-6e-+H2O=CO2+6H+.
3.在下列各组离子中,能大量共存的且溶液呈无色是( )
| A. | Na+、H+、Al3+、CH3COO- | B. | Mg2+、HCO3-、Ca2+、NO3- | ||
| C. | K+、SO42-、Cl-、Cu2+ | D. | NH4+、Cl-、K+、OH- |
20.当今人类利用的常规能源是( )
| A. | 化石燃料 | B. | 太阳能 | C. | 核能 | D. | 潮汐能 |
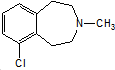 )一种治疗心血管和高血压的药物,可由化合物B(
)一种治疗心血管和高血压的药物,可由化合物B( )通过以下路线合成:
)通过以下路线合成: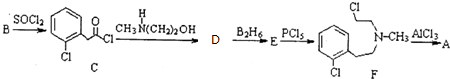
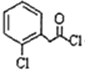 +CH3NH(CH2)2OH→
+CH3NH(CH2)2OH→ +HCl.
+HCl. .由F生成A的反应类型为取代反应.
.由F生成A的反应类型为取代反应. 或
或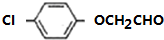 .
.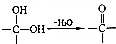 .写出以
.写出以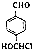 为原料制备化合物
为原料制备化合物 的合成路线流程图.
的合成路线流程图. .
.