题目内容
17.化学平衡发生移动的标志是各组分的百分含量发生变化,能够使化学平衡移动的因素有浓度、温度、压强,催化剂虽然能够加快速率,但不影响化学平衡移动.分析 正逆反应速率不等时平衡发生移动,各组分含量发生变化,常见影响平衡的因素有温度、浓度、压强等,催化剂同等程度的加快正逆反应速率,以此来解答.
解答 解:化学平衡发生移动的标志是各组分的百分含量发生变化,能够使化学平衡移动的因素有浓度、温度、压强;使用催化剂时,能降低反应的活化能,使单位体积内活化分子数目增多,从而加快反应速率,但不影响化学平衡移动,
故答案为:各组分的百分含量;浓度、温度、压强;加快;不影响.
点评 本题考查化学平衡移动原理,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握相关基础知识的积累,题目难度不大.

练习册系列答案
相关题目
7.化学与人类日常生活、生产密切相关.下列说法正确的是( )
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | 维生素C具有还原性,在人体内起抗氧化作用 | |
| C. | 侯氏制碱法的最终产品是小苏打 | |
| D. | 明矾可用于水的杀菌、消毒 |
1.2.0mol H2和1.0mol I2(g)充入体积不变的密闭容器中,在一定条件下发生下述反应:H2(g)+I2(g)?2HI(g),达平衡时,HI为0.40mol,如果此时移走1.0mol H2和0.50mol I2(g),在相同温度下再达到平衡时,HI的物质的量是( )
| A. | 0.40 mol | B. | 0.20 mol | ||
| C. | 小于0.20mol | D. | 大于0.20 mol,小于0.40 mol |
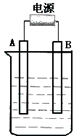 在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g.请回答下列问题:
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g.请回答下列问题: 已知A、B、C、D、E五种物质,且A、B、C、D的焰色反应均为黄色,它们的关系如下图所示,已知E为气体单质,能使带火星的木条复燃.
已知A、B、C、D、E五种物质,且A、B、C、D的焰色反应均为黄色,它们的关系如下图所示,已知E为气体单质,能使带火星的木条复燃.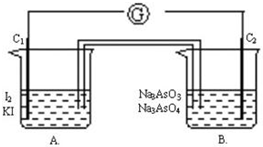 根据可逆反应:AsO43-+2I-+2H+?AsO33-+I2+H2O,设计如下图所示实验装置.
根据可逆反应:AsO43-+2I-+2H+?AsO33-+I2+H2O,设计如下图所示实验装置.