题目内容
a g Al2O3和CuO组成的混合物全部溶于20mL、物质的量浓度为0.1mol/L的盐酸中,反应后向所得溶液中加入10mL NaOH溶液,恰好使Cu2+、Al3+完全沉淀,则氢氧化钠溶液的物质的量浓度为( )
| A、0.1mol/L |
| B、0.2 mol/L |
| C、0.4mol/L |
| D、0.8mol/L |
考点:有关混合物反应的计算
专题:
分析:反应生成氯化铝、氯化铁,盐酸可能有剩余,向反应后的混合溶液中加入10mLNaOH溶液,恰好使Fe3+、Al3+完全沉淀,此时溶液中溶质为NaCl,根据钠离子守恒有n(NaOH)=n(NaCl),根据氯离子根守恒有n(NaCl)=n(HCl),据此计算n(NaOH),再根据c=
计算氢氧化钠溶液的物质的量浓度.
| n |
| V |
解答:
解:a g Al2O3和CuO组成的混合物全部溶于20mL、物质的量浓度为0.1mol/L的盐酸中,反应生成氯化铝、氯化铁,盐酸可能有剩余,
向反应后的混合溶液中加入10mLNaOH溶液,恰好使Fe3+、Al3+完全沉淀,此时溶液中溶质为NaCl,根据钠离子守恒有n(NaOH)=n(NaCl),
根据氯离子根守恒可得:n(NaCl)=n(HCl)=0.02L×0.1mol/L=0.002mol,
根据钠离子守恒有n(NaOH)=n(NaCl)=0.002mol,
则该NaOH溶液的物质的量浓度为:c(NaOH)=
=0.2mol/L,
故选B.
向反应后的混合溶液中加入10mLNaOH溶液,恰好使Fe3+、Al3+完全沉淀,此时溶液中溶质为NaCl,根据钠离子守恒有n(NaOH)=n(NaCl),
根据氯离子根守恒可得:n(NaCl)=n(HCl)=0.02L×0.1mol/L=0.002mol,
根据钠离子守恒有n(NaOH)=n(NaCl)=0.002mol,
则该NaOH溶液的物质的量浓度为:c(NaOH)=
| 0.002mol |
| 0.01L |
故选B.
点评:本题考查混合物计算、物质的量浓度有关计算,题目难度中等,注意利用守恒法解答,侧重对学生思维能力、分析处理问题能力的考查.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列两种气体的分子数一定相等的是( )
| A、质量相等、密度不等的N2和C2H4 |
| B、等体积等密度的CO和C2H4 |
| C、等温等体积的O3和N2 |
| D、等压等体积的N2和CO2 |
有关AgCl沉淀的溶解平衡的说法正确的是( )
| A、AgCl沉淀的生成和溶解在达到平衡时就不再进行 |
| B、AgCl不溶于水,溶液中没有Cl-和Ag+ |
| C、升高温度,AgCl的溶解度增大,Ksp增大 |
| D、向AgCl饱和溶液中加入NaCl固体,AgCl的溶解度和Ksp都不变 |
X、Y、Z、W、Q都是短周期元素,其中X原子的最外层电子数是内层电子数的3倍;X与Z同族,Y与Z同周期,Q原子的电子总数等于其电子层数的3倍,W与X、Y既不同族也不同周期且W不为稀有气体元素;X、Y、Z三种元素的族序数之和为16.下列说法正确的是( )
| A、Q与W能形成10电子,不能形成14电子、18电子分子 |
| B、Y的最高价氧化物对应水化物的化学式只能表示为H4YO4 |
| C、Y、Z、Q分别与X化合,只能形成AB2型化合物 |
| D、X、Z、W中的两种或三种元素形成的钠盐溶液可能显酸性、碱性、中性 |
实验室制备下列物质时,所用装置或方法正确的是( )
A、用SiO2和NaOH焙烧制备硅酸钠,可采用的图装置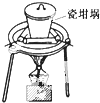 |
| B、制氧气时,用Na2O2或H2O2作反应物可选择相同的气体发生装置 |
| C、制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 |
| D、制二氧化氮时,用水或NaOH溶液吸收尾气 |
下列药品的水溶液,能用玻璃塞的无色玻璃试剂瓶贮存的是( )
| A、Na2SiO3 |
| B、NH4F |
| C、AgNO3 |
| D、H2SO4 |
化学与生活、社会密切相关.下列说法不正确的是( )
| A、乙醇是一种再生能源,充分燃烧的产物不污染环境 |
| B、凡含有食品添加剂的食物对人体健康均有害,不可食用 |
| C、为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术 |
| D、提倡人们购物时不用塑料袋,是为了防止白色污染 |
下列有关说法正确的是( )
| A、在101 kPa时,1molCH4完全燃烧生成CO2和水蒸气放出的热量就是CH4的燃烧热 |
| B、除去苯中混有的苯酚,可滴加浓溴水,再经过滤除去 |
C、已知:C-C、C=C、C-H、H-H键能分别为348,610,413,436(单位均为kJ/mol)则可以计算出反应 的△H为-384 kJ/mol 的△H为-384 kJ/mol |
| D、含1mol NaOH的稀溶液分别和含1mol CH3COOH、1molHNO3的稀溶液反应,前者比后者放出的热量少 |