题目内容
X、Y、Z、W、Q都是短周期元素,其中X原子的最外层电子数是内层电子数的3倍;X与Z同族,Y与Z同周期,Q原子的电子总数等于其电子层数的3倍,W与X、Y既不同族也不同周期且W不为稀有气体元素;X、Y、Z三种元素的族序数之和为16.下列说法正确的是( )
| A、Q与W能形成10电子,不能形成14电子、18电子分子 |
| B、Y的最高价氧化物对应水化物的化学式只能表示为H4YO4 |
| C、Y、Z、Q分别与X化合,只能形成AB2型化合物 |
| D、X、Z、W中的两种或三种元素形成的钠盐溶液可能显酸性、碱性、中性 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W、Q都是短周期元素,其中X原子的最外层电子数是内层电子数的3倍,最外层电子数不超过8个,则X内层电子数是2、最外层电子数是6,所以X是O元素;
X与Z同族,则Z是S元素;X、Y、Z三种元素的族序数之和为16,则Y族序数是4,Y和Z同周期,则Y是Si元素;
Q原子的电子总数等于其电子层数的3倍,如果Q有两个电子层,则Q是C元素,如果Q有3个电子层,则Q是F元素,F元素只有两个电子层,所以Q不是F元素,是C元素;
W与X、Y既不同族也不同周期且W不为稀有气体元素,则W是H元素,
再结合题目分析解答.
X与Z同族,则Z是S元素;X、Y、Z三种元素的族序数之和为16,则Y族序数是4,Y和Z同周期,则Y是Si元素;
Q原子的电子总数等于其电子层数的3倍,如果Q有两个电子层,则Q是C元素,如果Q有3个电子层,则Q是F元素,F元素只有两个电子层,所以Q不是F元素,是C元素;
W与X、Y既不同族也不同周期且W不为稀有气体元素,则W是H元素,
再结合题目分析解答.
解答:
解:X、Y、Z、W、Q都是短周期元素,其中X原子的最外层电子数是内层电子数的3倍,最外层电子数不超过8个,则X内层电子数是2、最外层电子数是6,所以X是O元素;
X与Z同族,则Z是S元素;X、Y、Z三种元素的族序数之和为16,则Y族序数是4,Y和Z同周期,则Y是Si元素;
Q原子的电子总数等于其电子层数的3倍,如果Q有两个电子层,则Q是C元素,如果Q有3个电子层,则Q是F元素,F元素只有两个电子层,所以Q不是F元素,是C元素;
W与X、Y既不同族也不同周期且W不为稀有气体元素,则W是H元素,
A.Q是C元素、W是H元素,Q与W能形成的CH4中含有10电子,C2H4中含有14电子、C2H6中含有18个电子,故A正确;
B.Y是Si元素,Y的最高价氧化物对应水化物的化学式能表示为H4YO4或H2YO3,故B错误;
C.C元素与O化合,能形成AB2型化合物,还能形成AB型化合物CO,故C错误;
D.O、S、H中的两种或三种元素形成的钠盐有硫酸钠、硫酸氢钠、亚硫酸钠、亚硫酸氢钠,硫酸氢钠溶液呈酸性,亚硫酸钠溶液呈碱性,硫酸钠溶液呈中性,所以O、S、H中的两种或三种元素形成的钠盐溶液可能显酸性、碱性、中性,故D正确;
故选D.
X与Z同族,则Z是S元素;X、Y、Z三种元素的族序数之和为16,则Y族序数是4,Y和Z同周期,则Y是Si元素;
Q原子的电子总数等于其电子层数的3倍,如果Q有两个电子层,则Q是C元素,如果Q有3个电子层,则Q是F元素,F元素只有两个电子层,所以Q不是F元素,是C元素;
W与X、Y既不同族也不同周期且W不为稀有气体元素,则W是H元素,
A.Q是C元素、W是H元素,Q与W能形成的CH4中含有10电子,C2H4中含有14电子、C2H6中含有18个电子,故A正确;
B.Y是Si元素,Y的最高价氧化物对应水化物的化学式能表示为H4YO4或H2YO3,故B错误;
C.C元素与O化合,能形成AB2型化合物,还能形成AB型化合物CO,故C错误;
D.O、S、H中的两种或三种元素形成的钠盐有硫酸钠、硫酸氢钠、亚硫酸钠、亚硫酸氢钠,硫酸氢钠溶液呈酸性,亚硫酸钠溶液呈碱性,硫酸钠溶液呈中性,所以O、S、H中的两种或三种元素形成的钠盐溶液可能显酸性、碱性、中性,故D正确;
故选D.
点评:本题考查原子结构和元素性质,正确推断元素是解本题关键,熟练掌握物质结构性质,知道常见10电子、18电子分子,易错点是Q元素判断,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
配制100mL1mol/L的氢氧化钠溶液,下列操作错误的是( )
| A、在托盘天平上放两片大小相同的纸,然后将氢氧化钠放在纸上称取 |
| B、把称得的氢氧化钠放入盛有适量蒸馏水的烧杯中,溶解、冷却,再把溶液转入容量瓶中 |
| C、用蒸馏水洗涤烧杯、玻棒2~3次,洗涤液也移入容量瓶 |
| D、沿着玻棒往容量瓶中加蒸馏水,直至溶液凹面的最低点与刻度相切 |
在一个6L的密闭容器内,通入2LX(气)和2LY(气),在一定条件下发生反应:4X(气)+3Y(气)?2Q(气)+nR(气).达平衡后,容器内温度不变,混合气体的压强比原来增大了5%,X的浓度减小到
,则该反应方程式中的n值是( )
| 1 |
| 3 |
| A、3 | B、4 | C、5 | D、6 |
下列装置能达到实验目的是( )
A、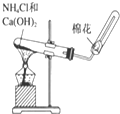 制取氨气 |
B、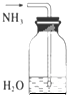 吸收多余氨气 |
C、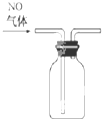 收集NO |
D、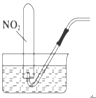 收集NO2 |
a g Al2O3和CuO组成的混合物全部溶于20mL、物质的量浓度为0.1mol/L的盐酸中,反应后向所得溶液中加入10mL NaOH溶液,恰好使Cu2+、Al3+完全沉淀,则氢氧化钠溶液的物质的量浓度为( )
| A、0.1mol/L |
| B、0.2 mol/L |
| C、0.4mol/L |
| D、0.8mol/L |
能用无色带玻璃塞的试剂瓶保存的物质是( )
| A、浓硝酸 | B、氢氧化钠溶液 |
| C、氯水 | D、醋酸 |
在一个密闭容器中充入1molCO2 和3molH2,在850℃时,气体混合物达到下式所示平衡:CO2+H2?CO+H2O.已知达到平衡时CO2的转化率为75%.那么当H2改为4mol,在上述条件下平衡时生成CO 和H2O的物质的量之和为( )
| A、1.5mol |
| B、1.8mol |
| C、1.6mol |
| D、2.5mol |