题目内容
在298K、101kPa时,充分燃烧一定量的丁烷,放出热量Q kJ(Q>0),经测定完全吸收生成的二氧化碳需要消耗5mol?L-1的KOH溶液100mL,恰好生成对应的酸式盐.则此条件下,下列热化学方程式正确的是( )
A、C4H10(g)+
| ||
B、C4H10(g)+
| ||
C、C4H10(g)+
| ||
D、C4H10(g)+
|
考点:反应热和焓变
专题:化学反应中的能量变化
分析:充分燃烧一定量的丁烷发生的反应为:2C4H10+13O2
8CO2+10H2O,CO2恰好与KOH溶液完全反应生成正盐为KHCO3,KOH+CO2═KHCO3,根据n=c×V计算KOH的物质的量,根据钾元素守恒计算n(KHCO3),根据碳元素守恒有n(CO2)=n(KHCO3),据此计算判断.
| ||
解答:
解:KOH的物质的量为n(KOH)=c×V=0.1L×5mol/L=0.5mol,
KOH+CO2═KHCO3,
根据钾离子守恒,故n(KHCO3)=0.5mol,
根据碳元素守恒由n(CO2)=n(KHCO3)=0.5mol,
2C4H10+13O2
8CO2+10H2O
根据碳元素守恒可知,丁烷的物质的量为n(C4H10)=0.5mol×
=
mol,
即
mol丁烷放出的热量大小为QkJ,
故1mol丁烷完全燃烧放出的热量为8QkJ,
则此条件下反应热化学方程式为C4H10(g)+
O2(g)═4CO2(g)+5H2O(l)△H=-8Q kJ?mol-1,
故选B.
KOH+CO2═KHCO3,
根据钾离子守恒,故n(KHCO3)=0.5mol,
根据碳元素守恒由n(CO2)=n(KHCO3)=0.5mol,
2C4H10+13O2
| ||
根据碳元素守恒可知,丁烷的物质的量为n(C4H10)=0.5mol×
| 1 |
| 4 |
| 1 |
| 8 |
即
| 1 |
| 8 |
故1mol丁烷完全燃烧放出的热量为8QkJ,
则此条件下反应热化学方程式为C4H10(g)+
| 13 |
| 2 |
故选B.
点评:本题考查反应热的计算,根据氢氧化钾确定丁烷的物质的量是解答该题的关键,题目难度中等.

练习册系列答案
相关题目
 一种从植物中提取的天然化合物a-damascone,可用于制作“香水”,其结构为(如下图)有关该化合物的下列说法不正确的是( )
一种从植物中提取的天然化合物a-damascone,可用于制作“香水”,其结构为(如下图)有关该化合物的下列说法不正确的是( )| A、该物质能与氢气发生加成反应 |
| B、该化合物可发生聚合反应 |
| C、1mol该化合物完全燃烧消耗19mol O2 |
| D、与溴的CCl4溶液反应生成的产物经水解、稀硝酸化后可用AgNO3溶液检验 |
 向密闭容器中充入物质A和B,发生反应aA(g)+bB(g)?cC(g).反应过程中,物质A的含量(A%)和C的含量(C%)随温度(T)的变化曲线如图所示,下列说法正确的是( )
向密闭容器中充入物质A和B,发生反应aA(g)+bB(g)?cC(g).反应过程中,物质A的含量(A%)和C的含量(C%)随温度(T)的变化曲线如图所示,下列说法正确的是( )| A、该反应在T1、T3温度时达到过化学平衡 |
| B、该反应在T2温度时达到过化学平衡 |
| C、该反应的逆反应是放热反应 |
| D、升高温度,平衡会向正反应方向移动 |
下列微粒的基态电子排布式书写错误的是( )
| A、镁原子:1s22s22p63s2 |
| B、铝离子:1s22s22p6 |
| C、S2-:1s22s22p63s23p4 |
| D、氟原子:1s22s22p5 |
把锌片和铁片放在盛有食盐水和酚酞的表面皿中,如图所示.最先观察到酚酞变红的现象的区域是( )

| A、Ⅰ和Ⅲ | B、Ⅰ和Ⅳ |
| C、Ⅱ和Ⅲ | D、Ⅱ和Ⅳ |
下列叙述正确的是( )
| A、阳离子都只有氧化性 |
| B、分子晶体中一定存在分子间作用力 |
| C、与强酸、强碱都反应的物质只有两性氧化物或两性氢氧化物 |
| D、分散系中分散质粒子的大小:Fe(OH)3悬浊液<Fe(OH)3胶体<FeCl3溶液 |
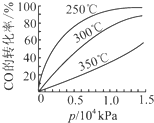 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.