��Ŀ����
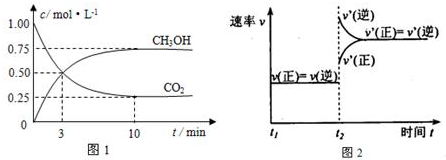
18��һ�������£���ɱ��ݻ����ܱ�������ͨ��N2��H2��������Ӧ��N2��g��+3H2��g��?2NH3��g����H��0���ﵽƽ������������Ϊ4L���Իش��������⣺
��1���������£���Ӧ��ƽ�ⳣ������ʽK=$\frac{{c}^{2}��N{H}_{3}��}{c��{N}_{2}��•{c}^{3}��{H}_{2}��}$���������¶ȣ�Kֵ���������������С�����䡱����
��2���ﵽƽ����������������䣬�����������Сһ�룬ƽ�⽫������Ӧ��������淴Ӧ������������Ӧ���������ƶ���ƽ�ⳣ�������䣮
��3���ﵽƽ����ں�ѹ�����£���������ͨ�뺤����He����������ת���ʽ���С�����������С�����䡱��
��4����������ͬ�������и�����1molN2��3molH2���ڲ�ͬ�����·ֱ�ﵽƽ�⣬���������������ʱ��仯������ͼ��ʾ������˵����ȷ����b������ţ�
a��ͼ������Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��p2��p1
b��ͼ�������ͬ��ͬѹ�£������Է�Ӧ��Ӱ�죬��������1��2
c��ͼ������Dz�ͬ�¶ȶԷ�Ӧ��Ӱ�죬��T1��T2
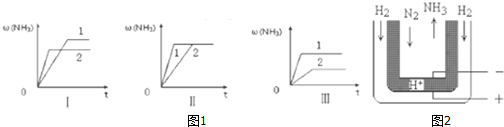
��5����ѹ�£���H2��Heϡ�͵�N2�ֱ�ͨ��һ��570��ĵ���װ�ã���ͼ2����H2��N2���ڵ缫�Ϻϳɰ���װ�������õĵ���ʣ�ͼ�к�ϸ�㣩�ܴ���H+���������ĵ缫��ӦΪN2+6H++6e-�T2NH3��
���� ��1����ѧƽ�ⳣ��K����������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ��÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ�ƽ�������ƶ�����ƽ�ⳣ��ֻ���¶��йأ�
��2���÷�Ӧ������Ӧ��һ����Ӧǰ�����������С�ķ�Ӧ������ѹǿ��ƽ�������������С�ķ����ƶ����¶Ȳ��䣬ƽ�ⳣ�����䣻
��3���ﵽƽ����ں�ѹ�����£���������ͨ�뺤�����μӷ�Ӧ�������ѹ��С��ƽ������������������ƶ���
��4��a������ѹǿƽ�����ƣ�
b��������Ӱ��ƽ���ƶ���
c�������¶�ƽ�������ƶ���
��5�����ص����������õ��ӵĻ�ԭ��Ӧ���ܷ�Ӧʽ��ȥ�����缫��Ӧʽ����Ϊ�����缫��Ӧʽ��
��� �⣺��1����ѧƽ�ⳣ��K����������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ����Ը÷�Ӧ��ƽ�ⳣ��K=$\frac{{c}^{2}��N{H}_{3}��}{c��{N}_{2}��•{c}^{3}��{H}_{2}��}$���÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ�ƽ�������ƶ�����ѧƽ�ⳣ������
�ʴ�Ϊ��$\frac{{c}^{2}��N{H}_{3}��}{c��{N}_{2}��•{c}^{3}��{H}_{2}��}$������
��2���÷�Ӧ������Ӧ��һ����Ӧǰ�����������С�ķ�Ӧ������ѹǿ��ƽ�������������С�ķ����ƶ���������Ӧ�����ƶ���
�ʴ�Ϊ��������Ӧ�����䣻
��3���ﵽƽ����ں�ѹ�����£���������ͨ�뺤�����μӷ�Ӧ�������ѹ��С��ƽ������������������ƶ������������ƶ���������ת���ʼ�С��
�ʴ�Ϊ����С��
��4��a������ѹǿƽ�����ƣ������ĺ���Ӧ����a����
b��������Ӱ��ƽ���ƶ�����ͼ���֪�������ܣ�1��2����b��ȷ��
c�������¶�ƽ�������ƶ��������ĺ�����С����c����
�ʴ�Ϊ��b��
��5���ܷ�ӦʽΪN2+3H2=2NH3�������ĵ缫��ӦΪ3H2-6e-�T6H+���ܷ�Ӧʽ��ȥ�����缫��Ӧʽ��Ϊ�����缫��Ӧʽ�����������缫��ӦʽΪ��N2+6H++6e-�T2NH3��
�ʴ�Ϊ��N2+6H++6e-�T2NH3��
���� ���⿼�黯ѧƽ���ƶ�Ӱ�����أ�Ϊ��Ƶ���㣬��ȷ�¶ȡ�Ũ�ȡ�ѹǿ�Ի�ѧƽ���ƶ�Ӱ��ԭ���ǽⱾ��ؼ���ע�⣺��ѧƽ�ⳣ��ֻ���¶��йأ�������Ũ�ȡ��������ѹǿ���أ���Ŀ�ѶȲ���

| A�� | 1.5 mol | B�� | 5.5 mol | C�� | 3 mol | D�� | 2.5 mol |
| A�� | a��b=3��1 | |
| B�� | X��Y��ת������� | |
| C�� | Y��Z����������֮��Ϊ2��3����ƽ���־ | |
| D�� | a��ȡֵ��ΧΪ0 mol•L-1��a��0.18 mol•L-1 |
| A�� | ������Һ������������Һ��H++SO42-+Ba2++OH-�TBaSO4��+H2O | |
| B�� | ������̼������Һ��ӦCO32-+2H+�TCO2��+H2O | |
| C�� | ��������Һ�м���ͭ��Ag++Cu�TCu2++Ag | |
| D�� | ����ϡ���ᷴӦ2Fe+6H+�T2Fe3++3H2�� |
| A�� | �����Ħ��������6.02��1023��������ӵ���������ֵ����� | |
| B�� | 6.02��1023��N2��6.02��1023��H2�������ȵ���14��1 | |
| C�� | 1 mol������1.5 mol����������ͬ��Ŀ����ԭ�� | |
| D�� | ���¡���ѹ�£�0.5��6.02��1023��һ����̼����������28 g |

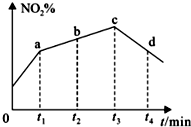 �о��������������ڴ����еĺ������ӵ������ʱ���漰���·�Ӧ��
�о��������������ڴ����еĺ������ӵ������ʱ���漰���·�Ӧ��