题目内容
10.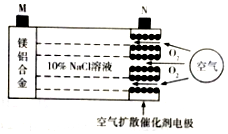 中科院宁波材料所研发金属空气电池获得重大突破.该电池的工作原理如图所示:下列有关说法正确的是( )
中科院宁波材料所研发金属空气电池获得重大突破.该电池的工作原理如图所示:下列有关说法正确的是( )| A. | 电池工作时,负极附近溶液的pH升高 | |
| B. | 电池工作时,电流由M极经外电路流向N极 | |
| C. | 电路中转移2mol电子,理论上约消耗标准状况下空气56L | |
| D. | 电池总反应为4Al+3O2=2Al2O3、2Mg+O2=2MgO |
分析 根据原电池的工作原理可以看出:活泼金属镁和铝的合金是负极,该电极上发生失电子的氧化反应,正极上是氧气得电子的还原反应,电子从负极流向着正极,电流从正极流向负极,总反应是正极和负极反应的和,根据电极反应式来回答.
解答 解:A、根据原电池的工作原理可以看出:活泼金属镁和铝的合金是负极,该电极上发生失电子的氧化反应,即Mg-2e-=Mg2+,正极上是氧气得电子的还原反应,产生氢氧根离子,氢氧根离子和镁离子之间反应会得到氢氧化镁,负极附近溶液的pH降低,故A错误;
B、电池工作时,电流从正极流向负极,即由N极经外电路流向M极,故B错误;
C、电路中转移2mol电子,根据正极上发生反应:O2+4H++4e-=2H2O,消耗氧气的物质的量是0.5mol,标况下的体积是11.2L,理论上约消耗标准状况下空气56L,故C正确;
D、电池总反应为2Mg+O2+2H2O=2Mg(OH)2↓,故D错误.
故选C.
点评 本题综合考查原电池知识,为高频考点,侧重于学生的分析能力的考查,侧重于正负极的判断和电极方程式的书写,学生要注意相关基础知识的积累,题目难度不大.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
20.化学反应速率与限度与生产、生活密切相关
(1)某学生为了探究锌与盐酸反应过程中的速率变化,他在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大2~3min,原因是该反应是放热反应,此时温度高,反应速率越大.
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率0.025mol/(L•min).
(设溶液体积不变)
(2)另一学生也做同样的实验,由于反应太快,不好控制测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是CD.
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)某温度下在4L密闭容器中,3种气态物质 X、Y、Z的物质的量随时间变化曲线如右图.
①该反应的化学方程式是3X+Y?2Z.
②在5min时,该反应达到了平衡状态,下列可作为判断反应已达到该状态的是CD.
A.X、Y、Z的反应速率相等
B.X、Y的反应速率比为3:1
C.容器内气体压强保持不变
D.生成1mol Y的同时生成2mol Z
③2min内X的转化率为30%.
④若上述反应中X、Y、Z分别为H2、N2、NH3,且已知17g氨气分解成氮气和氢气要吸收46kJ热量,则该反应的热化学反应方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92kJ/mol.
(1)某学生为了探究锌与盐酸反应过程中的速率变化,他在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 100 | 240 | 464 | 576 | 620 |
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率0.025mol/(L•min).
(设溶液体积不变)
(2)另一学生也做同样的实验,由于反应太快,不好控制测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是CD.
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)某温度下在4L密闭容器中,3种气态物质 X、Y、Z的物质的量随时间变化曲线如右图.

①该反应的化学方程式是3X+Y?2Z.
②在5min时,该反应达到了平衡状态,下列可作为判断反应已达到该状态的是CD.
A.X、Y、Z的反应速率相等
B.X、Y的反应速率比为3:1
C.容器内气体压强保持不变
D.生成1mol Y的同时生成2mol Z
③2min内X的转化率为30%.
④若上述反应中X、Y、Z分别为H2、N2、NH3,且已知17g氨气分解成氮气和氢气要吸收46kJ热量,则该反应的热化学反应方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92kJ/mol.
1.100mL 1mol•L-1Al2(SO4)3溶液中,含Al3+离子的物质的量( )
| A. | 0.1mol | B. | 0.2mol | C. | 0.3mol | D. | 0.4mol |
18.化学与生产和日常生活有着密切的关系,下列说法不科学或做法不正确的是( )
①明矾净水和漂白粉净水的原理相同
②电解MgCl2饱和溶液可以制得金属镁
③工厂里用静电除尘的原理与外科用FeCl3溶液应急止血的原理都与胶体的性质有关
④水玻璃是纯净物,是制造硅胶和木材防火剂的原料
⑤小苏打在医疗上常用作胃酸中和剂
⑥水晶项链和太阳能光电池的成分都是二氧化硅.
①明矾净水和漂白粉净水的原理相同
②电解MgCl2饱和溶液可以制得金属镁
③工厂里用静电除尘的原理与外科用FeCl3溶液应急止血的原理都与胶体的性质有关
④水玻璃是纯净物,是制造硅胶和木材防火剂的原料
⑤小苏打在医疗上常用作胃酸中和剂
⑥水晶项链和太阳能光电池的成分都是二氧化硅.
| A. | ①③④ | B. | ②③⑤⑥ | C. | ①②④⑥ | D. | ①③⑥ |
5.下列反应氯元素只被氧化的是( )
| A. | 5Cl2+I2+6H2O=10HCl+2HIO3 | B. | MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+H2O | ||
| C. | 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O | D. | 2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑ |
2.既能通过金属单质与足量Cl2反应得到,也能通过金属单质与酸反应得到的是( )
| A. | FeCl2 | B. | NaCl | C. | FeCl3 | D. | CuCl2 |
 ④
④ ⑤
⑤